Виды электролитов и особенности их использования. Электролитов видыОбщая характеристика электролитовОдни электролиты в растворах полностью распадаются на ионы. Они называются сильными. Другие электролиты только частично распадаются на ионы, т.е. большая часть их молекул остаётся в растворе в недиссоциированном виде. Такие электролиты называются слабыми. Данное свойство вещества не абсолютно, и зависит не только от его природы, но и от природы растворителя. Чем больше диэлектрическая постоянная растворителя, тем сильнее его ионизирующая слабость. Так, в водных растворах (ε(Н2О) = 80).LiClиNaClведут себя как сильные электролиты. Но если их растворить в уксусной кислоте (ε = 6) или ацетоне (ε = 21), то они начинают проявлять свойства слабых электролитов. В водных растворах сильными электролитами являются соли, растворимые основания (образованные, как правило, щелочными и щелочноземельными металлами), некоторые неорганические или минеральные кислоты (HCl, HBr, HI, h3SO4, HNO3 и др.). В тоже время многие органические кислоты, некоторые неорганические кислоты (HNO2, HF, h3S, h3SiO3, h4PO4 и т.д.), нерастворимые в Н2О основания ведут себя как слабые электролиты. Вещества, в которых частицы связаны различными видами химической связи, распадаются на ионы сперва по ионным связям KНSO4K++ НSO4–, а затем – по наиболее полярным ковалентным связям НSO4–Н++SO42–. Гетеролитический разрыв малополярных или неполярных ковалентных связей в процессах диссоциации таких веществ, как правило, не происходит. Количественно процесс распада молекул электролита на ионы оценивается с помощьюстепени электролитической диссоциации α. Степень диссоциации – это отношение числа распавшихся на ионы молекул вещества к общему числу его молекул в растворе (распавшихся и нераспавшихся):
NО=NД+NH (число непродиссоциированных молекул электролита в растворе) Так как число частиц вещества (N) и их химическое количество (n) связаны между собой соотношениемN=n∙NA, то степень диссоциации можно ещё рассчитать и другим способом:
Для сильных электролитов α близка к единице. Практически все их молекулы в растворе находятся в диссоциированном виде, процесс ассоциации протекает крайне незначительно. В связи с этим в уравнениях диссоциации данных веществ вместо знака обратимости «» ставят знак «» (т.е. используют стрелку только в направлении распада), например: HClH+ + Cl– KOНK+ + OH– K2SO42K++SO42– Слабые электролитыДля слабых электролитов степень диссоциации очень мала (α<<1). Так, для воды при 20оС α ≈ 1 ∙ 10–9. Это означает, что только одна молекула из миллиарда распадается на ионы. В растворах слабых электролитов, наряду с диссоциацией, непрерывно протекает и обратный процесс – ассоциация. С течением времени между ними устанавливается химическое равновесие, которое может быть смещено в ту или иную сторону. В результате диссоциации электролита происходит увеличение числа его частиц в растворе. Это позволяет экспериментально определить степень диссоциации по измерению тех свойств раствора, которые зависят только от количества содержащихся в нём частиц растворённого вещества, но не от их природы, размеров, массы. К таким свойствам относятся температура кипения и замерзания раствора, осмотическое давление и некоторые другие. Для растворов слабых электролитов значения α, определённые различными способами, как правило, совпадают и всегда значительно меньше единицы, что хорошо согласуется с теорией Аррениуса. Как показали экспериментальные исследования, степень диссоциации слабых электролитов зависит от температуры раствора и его концентрации. Таблица 8.Изменение степени диссоциации уксусной кислоты в зависимости от ее молярной концентрации в растворе
При повышении температуры раствора степень диссоциации увеличивается, т.к. при этом лучше обеспечивается поляризация и облегчается последующий разрыв ковалентной полярной связи в молекулах электролита. При понижении температуры α уменьшается. Возрастает α и при уменьшении концентрации растворов, т.е. при их разбавлении (табл. 8), т.к. при этом толщина разделяющей ионы водной прослойки становится больше, поэтому электростатическое взаимодействие между ними, приводящее к ассоциации ионов в молекулы, наблюдается реже. При бесконечно большом разведении степень диссоциации электролита стремится к своему максимальному значению, т.е. к единице (рис. 30). Рис. 30. Изменение степени электролитической диссоциации α с разбавлением V(схема) Таким образом, для слабых электролитов α не является постоянной величиной. Поэтому их способность к распаду на ионы удобнее сравнивать по константе диссоциации, которая представляет собой константу равновесия обратимой реакции электролитического разложения молекул электролита. Например: HNO2 H+ + NO2–
где СН+, СNO2–, CHNO2 – равновесные молярные концентрации ионов H+, NO2– и непродиссоциированных молекул HNO2. Константа диссоциации слабых электролитов не зависит от их концентрации в растворе даже при значительном разбавлениии и при данной температуре остается постоянной величиной (табл. 9). С увеличением температуры раствора константа диссоциации слабых электролитов во многих случаях изменяется сложным образом (рис. 31). Таблица 9.Зависимость величиныKдисс.уксусной кислоты в растворе от ее молярной концентрации при Т = 298K
Рис. 31. Зависимость константы диссоциации Kнекоторых слабых электролитов в водных растворах от температурыt(°С) Чем меньше Kдисс., тем более слабым является данный электролит. Например, уксусная кислота (Kдисс.= 1,85·10–5) почти в 220 000 раз сильнее циановодороднойHCN(Kдисс.= 4,8·10–10) и примерно в 10 раз слабее муравьиной кислоты (Kдисс.= 1,8·10–4). Существуют слабые электролиты (многоосновные кислоты, многокислотные основания) процесс распада которых на ионы протекает ступенчато, т.е. в несколько стадий. При этом каждая стадия характеризуется своей величиной константы диссоциации. Например, в 2 стадии осуществляется диссоциация сероводородной кислоты: 1) h3S H+ + HS– 2) HS– H+ + S2– Суммарное уравнение реакции диссоциации h3Sвыглядит следующим образом: h3S2H++S2– Величина константы диссоциации для суммарного уравнения и значения констант диссоциации отдельных стадий связаны между собой соотношением: Kсумм.=K1·K2·K3… При ступенчатой диссоциации распад слабого электролита на каждой последующей стадии происходит в меньшей степени, чем на предыдущей, т.е. K1>K2>K3 и т.д. Это объясняется тем, что отрыв иона происходит уже не от нейтральной молекулы (как на первой стадии), а от частицы со все более возрастающим зарядом и требует поэтому больших затрат энергии. Часто для оценки силы слабого электролита вместо величины константы диссоциации используют ее десятичный логарифм, взятый с обратным знаком (pK) pK= -lgKдисс. В этом случае чем больше величина pK, тем более слабым является электролит. Степень диссоциации слабого электролита уменьшается, если внести в его раствор даже в небольшом количестве сильный электролит, содержащий в своем составе одноименные ионы. Например, если в раствор СН3СООН добавить ацетат натрияCh4COONa, то за счет диссоциации соли концентрация ацетат-ионов СН3СОО–резко увеличится. В соответствии с принципом Ле Шателье это приведет к смещению равновесия реакции СН3СООНСН3СОО–+ Н+ в левую сторону. Аналогичный эффект наблюдается, если в раствор СН3СООН добавить небольшое количество сильной кислоты. Таким образом, диссоциация слабой кислоты подавляется в присутствии собственной соли или сильной кислоты. То же можно сказать и о слабом основании, диссоциация которого будет подавляться в сильнощелочной среде или в присутствии соли, содержащей одноименный катион. При добавлении большого количества соответствующего сильного электролита слабый электролит практически не будет диссоциировать. Существует количественная связь между степенью диссоциации слабого электролита и его концентрацией в растворе, называемая законом разбавления Оствальда. Для бинарного электролита, молекулы которого распадаются только на 2 иона, можно показать, что где С – исходная молярная концентрация электролита в растворе; α – степень диссоциации электролита; С ∙ α – концентрация распавшихся молекул электролита и образовавшихся при этом ионов. Вильгельм Фридрих Оствальд (1853 – 1932). Родился в Риге. Учился в Дерптском университете, здесь же в 1878 г. получил степень доктора. С 1882 г. был профессором Рижского университета. С 1887 г. перешел на кафедру физической химии в Лейпциге, где работал до 1928 г. В. Оствальд изучал электрическую проводимость органических кислот. Познакомившись с работами С. Аррениуса, он стал его сторонником. В. Оствальд внес существенный вклад в теорию электролитической диссоциации. В частности, он предложил свой известный закон разбавления, показал, что аналитические реакции в растворах следует рассматривать как ионные, и объяснил цвет растворов многих веществ специфической окраской ионов. В. Освальду принадлежат также исследования по катализу. Так как степень диссоциации слабых электролитов мала, то можно пренебречь этой величиной в знаменателе. Тогда K=C·α2, откудаили учитывая, что(разведение или разбавление раствора), то. Для электролитов, молекулы или формульные единицы которых распадаются на большее число ионов, закон разбавления Оствальда носит более сложный характер. studfiles.net примеры. Состав и свойства электролитов. Сильные и слабые электролитыЭлектролиты как химические вещества известны с древних времён. Однако большинство областей своего применения они завоевали относительно недавно. Мы обсудим самые приоритетные для промышленности области использования этих веществ и разберёмся, что же последние собой представляют и чем отличаются друг от друга. Но начнём с экскурса в историю.
ИсторияСамые старые известные электролиты - это соли и кислоты, открытые ещё в Древнем мире. Однако представления о строении и свойствах электролитов развивались со временем. Теории этих процессов эволюционировали, начиная с 1880 годов, когда был сделан ряд открытий, связанный с теориями свойств электролитов. Наблюдались несколько качественных скачков в теориях, описывающих механизмы взаимодействия электролитов с водой (ведь только в растворе они приобретают те свойства, благодаря которым их используют в промышленности). Сейчас мы подробно разберём несколько теорий, оказавших наибольшее влияние на развитие представлений об электролитах и их свойствах. И начнём с самой распространённой и простой теории, которую каждый из нас проходил в школе. Теория электролитической диссоциации Аррениусав 1887 году шведский химик Сванте Аррениус и русско-немецкий химик Вильгельм Оствальд создали теорию электролитической диссоциации. Однако тут тоже не всё так просто. Сам Аррениус был сторонником так называемой физической теории растворов, которая не учитывала взаимодействие составляющих вещества с водой и утверждала, что в растворе существуют свободные заряженные частицы (ионы). Кстати, именно с таких позиций сегодня рассматривают электролитическую диссоциацию в школе. Поговорим всё-таки о том, что даёт эта теория и как она объясняет нам механизм взаимодействия веществ с водой. Как и у любой другой, у неё есть несколько постулатов, которые она использует: 1. При взаимодействии с водой вещество распадается на ионы (положительный - катион и отрицательный - анион). Эти частицы подвергаются гидратации: они притягивают молекулы воды, которые, кстати, заряжены с одной стороны положительно, а с другой - отрицательно (образуют диполь), в результате формируются в аквакомплексы (сольваты). 2. Процесс диссоциации обратим - то есть если вещество распалось на ионы, то под действием каких-либо факторов оно вновь может превратиться в исходное. 3. Если подключить к раствору электроды и пустить ток, то катионы начнут движение к отрицательному электроду - катоду, а анионы к положительно заряженному - аноду. Именно поэтому вещества, хорошо растворимые в воде, проводят электрический ток лучше, чем сама вода. По той же причине их назвали электролитами. 4. Степень диссоциации электролита характеризует процент вещества, подвергшегося растворению. Этот показатель зависит от свойств растворителя и самого растворённого вещества, от концентрации последнего и от внешней температуры. Вот, по сути, и все основные постулаты этой несложной теории. Ими мы будем пользоваться в этой статье для описания того, что же происходит в растворе электролита. Примеры этих соединений разберём чуть позже, а сейчас рассмотрим другую теорию.
Теория кислот и оснований ЛьюисаПо теории электролитической диссоциации, кислота - это вещество, в растворе которого присутствует катион водорода, а основание - соединение, распадающееся в растворе на гидроксид-анион. Существует другая теория, названная именем известного химика Гилберта Льюиса. Она позволяет несколько расширить понятие кислоты и основания. По теории Льюиса, кислоты - это ионы или молекулы вещества, которые имеют свободные электронные орбитали и способны принять электрон от другой молекулы. Несложно догадаться, что основаниями будут являться такие частицы, которые способны отдать один или несколько своих электронов в "пользование" кислоте. Очень интересно здесь то, что кислотой или основанием может быть не только электролит, но и любое вещество, даже нерастворимое в воде.
Протолитическая теория Брендстеда-ЛоуриВ 1923 году, независимо друг от друга, двое учёных - Й. Бренстед и Т. Лоури -предложили теорию, которая сейчас активно применяется учёными для описания химических процессов. Суть этой теории в том, что смысл диссоциации сводится к передаче протона от кислоты основанию. Таким образом, последнее понимается здесь как акцептор протонов. Тогда кислота является их донором. Теория также хорошо объясняет существование веществ, проявляющих свойства и кислоты и основания. Такие соединения называются амфотерными. В теории Бренстеда-Лоури для них также применяется термин амфолиты, тогда как кислота или основания принято называть протолитами. Мы подошли к следующей части статьи. Здесь мы расскажем, чем отличаются друг от друга сильные и слабые электролиты и обсудим влияние внешних факторов на их свойства. А затем уже приступим к описанию их практического применения. Сильные и слабые электролитыКаждое вещество взаимодействует с водой индивидуально. Какие-то растворяются в ней хорошо (например, поваренная соль), а какие-то совсем не растворяются (например, мел). Таким образом, все вещества делятся на сильные и слабые электролиты. Последние представляют собой вещества, плохо взаимодействующие с водой и оседающие на дне раствора. Это означает, что они имеют очень низкую степень диссоциации и высокую энергию связей, которая не позволяет при нормальных условиях распадаться молекуле на составляющие её ионы. Диссоциация слабых электролитов происходит либо очень медленно, либо при повышении температуры и концентрации этого вещества в растворе. Поговорим о сильных электролитах. К ним можно отнести все растворимые соли, а также сильные кислоты и щёлочи. Они легко распадаются на ионы и очень трудно собрать их в осадки. Ток в электролитах, кстати, проводится именно благодаря ионам, содержащимся в растворе. Поэтому лучше всех проводят ток сильные электролиты. Примеры последних: сильные кислоты, щёлочи, растворимые соли.
Факторы, влияющие на поведение электролитовТеперь разберёмся, как влияет изменение внешней обстановки на свойства веществ. Концентрация напрямую влияет на степень диссоциации электролита. Более того, это соотношение можно выразить математически. Закон, описывающий эту связь, называется законом разбавления Оствальда и записывается так: a = (K / c)1/2. Здесь a - это степень диссоциации (берётся в долях), К - константа диссоциации, разная для каждого вещества, а с - концентрация электролита в растворе. По этой формуле можно узнать много нового о веществе и его поведении в растворе. Но мы отклонились от темы. Кроме концентрации, на степень диссоциации также влияет температура электролита. Для большинства веществ её увеличение повышает растворимость и химическую активность. Именно этим можно объяснить протекание некоторых реакций только при повышенной температуре. При нормальных условиях они идут либо очень медленно, либо в обе стороны (такой процесс называется обратимым). Мы разобрали факторы, определяющие поведение такой системы, как раствор электролита. Сейчас перейдём к практическому применению этих, без сомнения, очень важных химических веществ.
Промышленное использованиеКонечно, все слышали слово "электролит" применительно к аккумуляторам. В автомобиле используют свинцово-кислотные аккумуляторы, роль электролита в котором выполняет 40-процентная серная кислота. Чтобы понять, зачем там вообще нужно это вещество, стоит разобраться в особенностях работы аккумуляторов. Так в чём принцип работы любого аккумулятора? В них происходит обратимая реакция превращения одного вещества в другое, в результате которой высвобождаются электроны. При заряде аккумулятора происходит взаимодействие веществ, которого не получается при нормальных условиях. Это можно представить как накопление электроэнергии в веществе в результате химической реакции. При разряде же начинается обратное превращение, приводящее систему к начальному состоянию. Эти два процесса вместе составляют один цикл заряда-разряда. Рассмотрим вышеизложенный процесс на конкретном примере - свинцово-кислотном аккумуляторе. Как нетрудно догадаться, этот источник тока состоит из элемента, содержащего свинец (а также диокисд свинца PbO2) и кислоты. Любой аккумулятор состоит из электродов и пространства между ними, заполненного как раз электролитом. В качестве последнего, как мы уже выяснили, в нашем примере используется серная кислота концентрацией 40 процентов. Катод такого аккумулятора делают из диоксида свинца, а анод состоит из чистого свинца. Всё это потому, что на этих двух электродах протекают разные обратимые реакции с участием ионов, на которые продиссоциировала кислота:
Если читать реакции слева направо - получаем процессы, происходящие при разряде аккумулятора, а если справа налево - при заряде. В каждом химическом источнике тока эти реакции разные, но механизм их протекания в общем описывается одинаково: происходят два процесса, в одном из которых электроны "поглощаются", а в другом, наоборот, "выходят". Самое главное то, что число поглощённых электронов равно числу вышедших. Собственно, кроме аккумуляторов, существует масса применений этих веществ. Вообще, электролиты, примеры которых мы привели, - это лишь крупинка того многообразия веществ, которые объединены под этим термином. Они окружают нас везде, повсюду. Вот, например, тело человека. Думаете, там нет этих веществ? Очень ошибаетесь. Они находятся везде в нас, а самое большое количество составляют электролиты крови. К ним относятся, например, ионы железа, которые входят в состав гемоглобина и помогают транспортировать кислород к тканям нашего организма. Электролиты крови также играют ключевую роль в регуляции водно-солевого баланса и работе сердца. Эту функцию выполняют ионы калия и натрия (существует даже процесс, происходящий в клетках, который назвается калий-натриевым насосом). Любые вещества, которые вы в силах растворить хоть немного, - электролиты. И нет такой отрасли промышленности и нашей с вами жизни, где бы они ни применялись. Это не только аккумуляторы в автомобилях и батарейки. Это любое химическое и пищевое производство, военные заводы, швейные фабрики и так далее. Состав электролита, кстати, бывает разным. Так, можно выделить кислотный и щелочной электролит. Они принципиально отличаются своими свойствами: как мы уже говорили, кислоты являются донорами протонов, а щёлочи - акцепторами. Но со времением состав электролита меняется вследствие потери части вещества концентрация либо уменьшается, либо увеличивается (всё зависит от того, что теряется, вода или электролит). Мы каждый день сталкиваемся с ними, однако мало кто точно знает определение такого термина, как электролиты. Примеры конкретных веществ мы разобрали, поэтому перейдём к немного более сложным понятиям.
Физические свойства электролитовТеперь о физике. Самое важное, что нужно понимать при изучении этой темы - как передаётся ток в электролитах. Определяющую роль в этом играют ионы. Эти заряженные частицы могут переносить заряд из одной части раствора в другую. Так, анионы стремятся всегда к положительному электроду, а катионы - к отрицательному. Таким образом, действуя на раствор электрическим током, мы разделяем заряды по разным сторонам системы. Очень интересна такая физическая характеристика, как плотность. От неё зависят многие свойства обсуждаемых нами соединений. И зачастую всплывает вопрос: "Как поднять плотность электролита?" На самом деле ответ прост: необходимо понизить содержание воды в растворе. Так как плотность электролита большей частью определяется плотностью серной кислоты, то она большей частью зависит от концентрации последней. Существует два способа осуществить задуманное. Первый достаточно простой: прокипятить электролит, содержащийся в аккумуляторе. Для этого нужно зарядить его так, чтобы температура внутри поднялась чуть выше ста градусов по цельсию. Если этот способ не помогает, не переживайте, существует ещё один: просто-напросто заменить старый электролит новым. Для этого нужно слить старый раствор, прочистить внутренности от остатков серной кислоты дистиллированной водой, а затем залить новую порцию. Как правило, качественные растворы электролита сразу имеют нужную величину концентрации. После замены можете надолго забыть о том, как поднять плотность электролита. Состав электролита во многом определяет его свойства. Такие характеристики, как электропроводность и плотность, например, сильно зависят от природы растворённого вещества и его концентрации. Существует отдельный вопрос о том, сколько электролита в аккумуляторе может быть. На самом деле его объём напрямую связан с заявленной мощностью изделия. Чем больше серной кислоты внутри аккумулятора, тем он мощнее, т. е. тем большее напряжение способен выдавать.
Где это пригодится?Если вы автолюбитель или просто увлекаетесь автомобилями, то вы и сами всё понимаете. Наверняка вы даже знаете, как определить, сколько электролита в аккумуляторе находится сейчас. А если вы далеки от автомобилей, то знание свойств этих веществ, их применения и того, как они взаимодействуют друг с другом будет совсем не лишним. Зная это, вы не растеряетесь, если вас попросят сказать, какой электролит в аккумуляторе. Хотя даже если вы не автолюбитель, но у вас есть машина, то знание устройства аккумулятора будет совсем не лишним и поможет вам в ремонте. Будет гораздо легче и дешевле сделать всё самому, нежели ехать в автоцентр. А чтобы лучше изучить эту тему, мы рекомендуем почитать учебник химии для школы и вузов. Если вы хорошо знаете эту науку и прочитали достаточно учебников, лучшим вариантом будут "Химические источники тока" Варыпаева. Там изложены подробно вся теория работы аккумуляторов, различных батарей и водородных элементов. ЗаключениеМы подошли к концу. Подведём итоги. Выше мы разобрали всё, что касается такого понятия, как электролиты: примеры, теория строения и свойств, функции и применение. Ещё раз стоит сказать, что эти соединения составляют часть нашей жизни, без которой не могли бы существовать наши тела и все сферы промышленности. Вы помните про электролиты крови? Благодаря им мы живём. А что насчёт наших машин? С помощью этих знаний мы сможем исправить любую проблему, связанную с аккумулятором, так как теперь понимаем, как поднять плотность электролита в нём. Всё рассказать невозможно, да мы и не ставили такой цели. Ведь это далеко не всё, что можно рассказать об этих удивительных веществах. fb.ru Типы электролитов. Степень диссоциации.Стр 1 из 6Следующая ⇒РАБОТА 1. СВОЙСТВА РАСТВОРОВ Теоретическая часть Типы электролитов. Степень диссоциации. Электролиты – соли, кислоты, основания, имеющие полярные и ионные связи, – при растворении в воде в той или иной мере диссоциируют (распадаются на ионы). Для количественной характеристики соотношения диссоциированных и недиссоциированных молекул электролита пользуются понятием степени электролитической диссоциации (ионизации). Степень электролитической диссоциации α равна отношению числа (концентрации, Сд) диссоциированных молекул Nд. к общему числу (концентрации, Со) молекул Nо растворѐнного вещества:
Степень диссоциации электролита в водных растворах зависит от природы электролита, концентрации, наличия других растворѐнных веществ и температуры. Повышение температуры и уменьшение концентрации раствора увеличивает степень диссоциации, которая в бесконечно разбавленных растворах приближается к единице. По степени диссоциации электролиты условно можно разделить на три группы: сильные, средней силы и слабые. Принято считать сильными электролитами те, для которых α ≥ 30%, слабыми – если α ≤ 3% и средней силы – если 3% < α < 30%, причѐм все указанные значения α относятся к децимолярным (0,1 М) растворам электролитов при 25 оС. Более строгое разделение электролитов на сильные и слабые основано на значениях констант диссоциации. Сильные электролиты в водных растворах существуют только в виде ионов. Истинная степень их ионизации близка к 1 (100%), хотя экспериментально наблюдаемая (кажущаяся) находится в пределах от 30% и выше. Особенности поведения сильных электролитов, проявляющиеся в уменьшении их активности в электрохимических процессах, обусловлены электростатическим взаимодействием ионов друг с другом и с растворителем, уменьшением подвижности образующихся сложных ассоциатов. Электролитами средней силы являются некоторые органические и неорганические кислоты. К слабым электролитам принадлежат такие кислоты, как h3S, HCN, h4BO3, Ch4COOH, Н2СО3, гидроксид аммония Nh5OH, немногие соли (HgCl2, CdCl2, Fe(SCN)3). Вследствие незначительной диссоциации (α < 3%) слабые электролиты в ионных уравнениях с их участием пишутся в молекулярной форме. Экспериментально степень диссоциации можно определить по электропроводности, через изотонический коэффициент( эбулиоскопическим или криоскопическим методами), рН-метрически. mykonspekts.ru Тип - электролит - Большая Энциклопедия Нефти и Газа, статья, страница 1Тип - электролитCтраница 1 Тип электролита и массовая доля ( %) золота К, мОм ЯВ. [1] Тип электролита обозначен цифрами у кривых: первая цифра характеризует валентность катиона, вторая-валентность аниона. [3] Тип электролита обозначен цифрами у кривых: первая цифра характеризует валентность катиона, вторая-валентность аниона. [5] Тип электролита и его конвекция определяют собой величину предельного тока диффузии, а также возможность получения компактных или порошкообразных катодных отложений. [6] Тип электролита в элементе ( пятая колонка таблицы) также важен, поскольку он определяет внутреннее сопротивление элемента, а также скорость саморазряда. Саморазряд - это потребление энергии внутри элемента, которое уменьшает емкость элемента с течением времени после его изготовления. Элементы с жидким электролитом, как правило, имеют среднее значение внутреннего сопротивления и среднюю или низкую скорость саморазряда. Элементам с твердым электролитом, как правило, присущи более высокое внутреннее сопротивление и существенно более низкая скорость саморазряда. [7] Тип электролита обозначен цифрами у кривых: первая цифра характеризует валентность катиона, вторая-валентность аниона. [9] Тип электролита комплексного соединения определяют по следующей схеме. Исходя из формульной массы рассчитывают концентрацию и измеряют электрическую проводимость комплекса. Сравнение значений измеренной проводимости с табличными данными позволяет отнести электролит к тому или иному типу. [11] Этот тип электролитов для осаждения алюминия занимает наибольшее место в исследовании процесса электроосаждения алюминия, а различные модификации эфирно-гидридного электролита внедряются в производство. [12] Выбор типа электролита определяется характером исходного природного магниевого сырья. При питании магниевых ванн безводным карналитом ( KCl - MgCl2 - 6h3O) в ванне самопроизвольно образуется калиевый электролит. Применение натриево-калиевого электролита считается целесообразным, когда магниевым сырьем является практически чистый, безводный хлорид магния, например, получаемый из бишофита ( MgCl2 - 6h3O) или возвратный продукт из процесса термического восстановления титана. [14] Кроме типа электролита и растворителя, входящих в состав фона и определяющих продолжительность шкалы потенциалов, в которой можно получать полярографические волны исследуемых веществ, существенную роль в получении приемлемых для анализа волн играют и такие факторы, как значение рН фона и его буферная емкость. [15] Страницы: 1 2 3 4 www.ngpedia.ru Электрохимия –раздел физической химии, изучающий процессы взаимного превращения электрической и химической форм движения материи. Электрохимия рассматривает строение и свойства растворов электролитов, работу гальванических элементов, электрохимическую коррозию металлов, электросинтез веществ. Электролиты – это химические соединения, которые в соответствующем растворителе частично или полностью распадаются (диссоциируют) на ионы. Проводники электрического тока делятся на два типа: Проводники первого рода – перенос электричества обусловлен движением электронов. К ним относятся металлы и их сплавы в твердом и расплавленном состоянии. Проводники второго рода – перенос электричества обусловлен движением ионов под действием внешнего электрического поля. К ним относятся водные растворы кислот, щелочей, солей; растворы этих веществ в растворителях с электропроводящими свойствами, расплавленные соли и щелочи. Электропроводность проводников первого рода на несколько порядков выше, чем проводников второго рода. Смешанные проводники (растворы щелочных металлов в Nh4) – перенос электричества обусловлен движением ионов и сольватированных электронов, которые образуются при растворении щелочных металлов в аммиаке. Электрод – это проводник первого рода. С ростом температуры электрическое сопротивление этих проводников растет (тепловые колебания кристаллической решетки). Растворы электролитов - проводники второго рода. Электрическое сопротивление этих проводников с ростом температуры падает (уменьшается вязкость среды). Если электролит распадается на два иона, он называется бинариным или симметричным. При этом тип электролита определяется по его валентности. Например, KCl K+1 + Cl-1 1, 1-валентный электролит CuSO4 Cu2+ + SO42- 2,2 - валентный электролит Несимметричные электролиты также определяются по валентности. K2 SO4 2K+ + SO42- 1,2 - валентный электролит CoCI3 Co3+ + 3CI- 3,1 - валентный электролит Электролитическая диссоциация (Ионные равновесия в растворах электролитов)Базовой для этих равновесий является теория Аррениуса, которая в основном не потеряла своей актуальности до сих пор. Основные положения теории Аррениуса: 1.Диссоциация электролита на ионы в растворе идет самопроизвольно, независимо от того протекает или нет электрический ток через раствор. 2.Для слабых электролитов диссоциация имеет динамический характер.
(К - катион, А - анион) В результате этого процесса устанавливается равновесие, характеризуемое степенью и константой диссоциации. 3.Ионы в растворе ведут себя аналогично молекулам идеального газа (в отличие от первых двух, последний пункт полностью неверный). Механизм диссоциацииНаиболее универсальным растворителем является вода, молекула которой имеет несимметричное строение. Возьмем ионный кристалл NaCl и поместим в воду. Полярные молекулы воды ориентируются противоположно заряженным ионам кристаллической решетки и вырывают их с поверхности. Ион кристалла переходит в раствор, где окружается молекулами растворителя. Этот процесс, в случае если растворитель вода, называется гидратацией, если любой другой растворитель – сольватацией. Энергия взаимодействия между ионами в кристалле достигает сотен кДж/моль. Энергия, необходимая для разрыва этих связей, поставляется за счет гидратации (сольватации), которая протекает с выделением энергии. В зависимости от соотношения энергии разрыва связей в исходном электролите и энергии гидратации при растворении, раствор может либо нагреваться, либо охлаждаться. Согласно закону Кулона: - сила взаимодействия между ионами в кристаллической решетке электролита обратно пропорциональна диэлектрической проницаемости растворителя (ε). z+, z- - заряды катиона и аниона; r- равновесное расстояние между ними. вакуум =1 Поэтому взаимодействие между ионами в воде ослаблено почти в 80 раз по отношению к этому взаимодействию в кристалле. Диссоциирующая способность растворителя прямо пропорциональна его диэлектрической проницаемости. studfiles.net 1. Ионизация в ионных соединениях.
14 РАСТВОРЫ ЭЛЕКТРОЛИТОВ Электролит – это вещество, которое при определенных условиях способно распадаться на заряженные частицы, называемые ионами. Под определенными условиями может подразумеваться раствор, расплав, распад на ионы под действием температуры (термодиссоциация CaCO3 CaO + CO2), в плазме и фотодиссоциация – разложение веществ под действием ионизирующего излучения (Cl22Cl). Раствор электролита – это раствор, который способен проводить электрический ток. КЛАССИФИКАЦИЯ ЭЛЕКТРОЛИТОВ
Диссоциация электролитов наблюдается в полярных растворителях и зависит от их диэлектрической проницаемости . Чем выше значение диэлектрической проницаемости, тем полнее диссоциация. Большая диэлектрическая проницаемость наблюдается для воды (при 25 0С =78,3). Лишь незначительное количество неводных растворов, например, формамид, имеют диэлектрическую проницаемость выше, чем у воды. Растворы электролитов в подобных растворителях обладают высокой электрической проводимостью. В неполярных растворителях, таких как четыреххлористый углерод (=2,238), электролитической диссоциации практически не происходит. В зависимости от числа образующихся в результате электролитической диссоциации катионов и анионов различают симметричные и несимметричные электролиты. ЭЛЕКТРОЛИТЫ
ТЕОРИЯ СЛАБЫХ ЭЛЕКТРОЛИТОВ. СТЕПЕНЬ И КОНСТАНТА ДИССОЦИАЦИИ. Первая количественная теория растворов электролитов (теория электролитической диссоциации) была высказана Аррениусом. По этой теории молекулы электролитов при растворении распадаются на противоположно заряженные ионы. Процесс диссоциации слабого электролита обратим, т.е. наряду с диссоциацией молекул происходит образование молекул из ионов и, таким образом, в растворе наряду с ионами существуют и молекулы. Доля молекул, распадающихся на ионы, оценивается степенью электролитической диссоциации, которую обычно обозначают . Степень диссоциации – это отношение числа молекул, распавшихся на ионы, к числу молекул растворенного вещества.
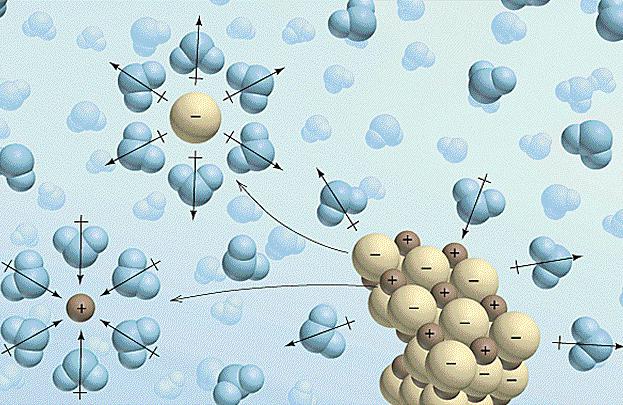
Степень диссоциации является характеристикой электролита: Для неэлектролитов (сахароза) = 0; Для сильных электролитов ≥ 1; Для слабых электролитов 0 < < 1. Рассмотрим диссоциацию уксусной кислоты: СН3СООНН++ СН3СОО- Так как процесс диссоциации слабого электролита обратим, то он характеризуется константой равновесия. Константа равновесия для процесса диссоциации есть константа диссоциации. Т.е. все закономерности, характерные для константы равновесия, справедливы и для константы диссоциации. . Константа диссоциации зависит от природы растворителя и температуры (=f(Т)), но не зависит от концентрации электролита в растворе (f(С)). Зависимость константы диссоциации от температуры описывается уравнением изобары Вант-Гоффа: . Пусть концентрация растворенной уксусной кислоты будет С, а степень диссоциации равна . Тогда ,;;. Подставим эти значения в выражение константы диссоциации: ; - аналитическое выражение закона разбавления Оствальда, где С – общая концентрация электролита [моль/дм3]. Рассмотрим очень слабый электролит, степень диссоциации которого намного меньше единицы (<<1). Тогда закон разбавления Оствальда преобразуется: . Как видно, степень диссоциации обратно пропорциональна корню квадратному из концентрации электролита. Чем больше концентрации, тем меньше степень диссоциации. В связи с этим вводится понятие бесконечно разбавленного раствора, в котором даже слабые электролиты полностью диссоциируют на ионы и отсутствуют силы электростатического взаимодействия. ПРИЧИНЫ И МЕХАНИЗМ ИОНИЗАЦИИ В ВОДНЫХ РАСТВОРАХ К ионным соединениям относятся в основном соли с ионной кристаллической решеткой. Такие соединения состоят из ионов не только в растворе, но и в кристаллическом и парообразном состоянии: NaCl Na + Cl Na+Cl- Молекула воды полярна из-за разности электроотрицательности кислорода и водорода. Молекула воды имеет угловое строение. Кислород оттягивает на себя электронную плотность, так как его электроотрицательность выше, чем у водорода. На атоме кислорода возникает двойной частично отрицательный заряд, а на каждом из двух атомов водорода частично положительный заряд. Поэтому молекула воды поляризована и её можно представить в виде диполя. Диполи воды подходят к ионам электролита в кристаллической решетке, ориентируются в его электростатическом поле и ослабляют взаимодействие между ионами в кристалле. Происходит отрыв иона, его гидратация, то есть электролит растворяется в воде. 2. Диссоциация полярных соединений.Кроме гидратации (сольватации) важным фактором, приводящим к диссоциации электролита, является способность молекул растворителя образовывать разного типа связи с частицами электролита.
Например, молекулы воды обладают способностью образовывать водородные связи не только между собой, но и с другими молекулами, содержащими атомы сильно отрицательных элементов, таких как фтор, кислород, азот, хлор и другие. Например, при растворении в воде хлороводорода происходит ориентация диполей воды вокруг растворенных молекул, вызывающая ещё большую поляризацию молекул хлороводорода.
Полярная связь между атомами водорода и хлора переходит в ионную. При этом общая электронная пара целиком сдвигается к атому хлора, и в результате происходит гетеролитический разрыв молекулы. Атом хлора превращается в гидратированный хлорид-ион, а протон с молекулой воды образует сложную положительно заряженную частицу h4O+, называемую гидроксонием. HCl + xh3O = h4O+ + Cl-(x-1)h3O Так как гидратированная частица h4O+ и гидратированный хлорид-ион в уравнении электролитической диссоциации могут быть заменены знаками иона водорода и хлора, то уравнение можно записать так: HCl = Н+ + Cl-. ТЕОРИЯ СЛАБЫХ ЭЛЕКТРОЛИТОВ АРРЕНИУСА По этой теории:
Пользуясь теорией Аррениуса, нельзя было объяснить, почему разные методы определения константы диссоциации для некоторых электролитов дают разные значения, почему для ряда электролитов константа диссоциации зависит от концентрации раствора. А также тот экспериментальный факт, что для некоторых электролитов при высоких концентрациях раствора степень диссоциации получалась больше единицы. Теория не указывает причин, вызывающих диссоциацию молекул на ионы, и не объясняет, за счет каких сил она происходит. Поэтому существует ещё одна теория – теория сильных электролитов Кольрауша. ТЕОРИЯ СИЛЬНЫХ ЭЛЕКТРОЛИТОВ КОЛЬРАУША По этой теории:
ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРОВ ЭЛЕКТРОЛИТОВ Растворы электролитов – это проводники 2 рода, обладающие ионной проводимостью. Количественной характеристикой способности растворов переносить электрический ток является электропроводность. Электропроводность – это величина, обратная сопротивлению. , - сопротивление, где R – сопротивление [Ом]; - удельное сопротивление [Ом·м]; l – длина проводника [м]; S – площадь поперечного сечения [м2]. Различают два вида электропроводности:
æ=, [Ом-1·м-1] = [См/м], где См [Сименс=]. Удельная электрическая проводимость раствора электролита – это электрическая проводимость объема раствора, заключенного между двумя параллельными электродами, имеющими площадь по 1 м2 и расположенными на расстоянии 1 м друг от друга. Величина удельной электропроводности прямо пропорционально зависит от концентрации ионов в единице объема, скорости их движения и переносимого каждым ионом заряда.
Молярная электрическая проводимость раствора – мера электрической проводимости всех ионов, образующихся при диссоциации 1 моль электролита при данной концентрации. Молярная электропроводность – это электрическая проводимость объема раствора V(м3), заключенного между двумя параллельными электродами, с межэлектродным расстоянием 1 м, причем каждый электрод имеет такую площадь, чтобы в этом объеме содержался 1 моль растворенного вещества. Между молярной и удельной электрическими проводимостями имеется соотношение =æV=æ/C, где - молярная электрическая проводимость, См·м2/моль; æ – удельная электрическая проводимость, См/м; V – разведение раствора, м3/моль; С – концентрация, моль/м3. Если концентрация раствора выражена в моль/дм3, а æ – в См/см, то это уравнение записывается в виде =1000·æ/С. Электропроводность зависит от:
studfiles.net Виды электролитов и особенности их использования
Жидкости, проводящие электричество, называются электролитами. К ним относятся не только растворы, но и расплавы твердых веществ. Области примененияЭлектролиты применяются во многих отраслях хозяйства.
Интернет-магазин «Фармконтракт – Дистрибьюторское подразделение» предлагает уникальные приборы для электрохимических измерений, надежные и простые в эксплуатации. Плюсы и минусы щелочных электролитовСамый распространенный способ использования электролитов – аккумуляторы для транспортных средств. Щелочные электролиты – это растворы щелочей. Чаще всего используются гидроокиси самых активных металлов - натрия, калия, лития. Использование щелочных электролитов имеет много плюсов:
Однако их применение ограничено несколькими условиями:
И самое главное – щелочные электролиты не могут обеспечить силу тока, способную завести автомобильный мотор. Они применяются, в основном, в электровозах на железных дорогах и в шахтах. Кислотные электролитыКислотным электролитом служит раствор серной кислоты высокой концентрации, такой аккумулятор мощнее щелочного, он имеет:
Неудобство в работе с кислотным электролитом создает:
Для автомобилей больше подходят кислотные аккумуляторы. Совместная зарядка кислотных и щелочных аккумуляторов запрещена, она может привести к взрыву в помещении. Нельзя также заливать щелочной электролит в кислотный аккумулятор и наоборот. Ассортимент оборудования для электрохимических методов анализа представлен в нашем интернет-магазине достаточно широко. Видео. Что такое электролит. phct-lab.ru |
|
||||||||||||||||||
|
|
||||||||||||||||||
|