Содержание
Ацетон ГОСТ бочка | e-shop НЕФРАС КОМ
Ацетон — (2-пропанон, диметилкетон) прозрачная жидкость с характерным запахом, имеющая формулу Ch4—C(O)—Ch4. Очень летучее и химически стабильное вещество. Смешивается с водой и органическими растворителями. Ацетон относится к кетонам, которые используются в качестве растворителей. Является очень активным растворителем многих смол и жиров. Ацетон изготавливается по ГОСТ 2768-84.
Ацетон используется в качестве сильного летучего растворителя в быстросохнущих целлюлозных лаках,в клеях как экстрагирующее вещество и детергент, как агент набухания для нитроцеллюлозы при производстве бездымного пороха. Как растворитель при производстве пленок на основе нитрата целлюлозы. Применяется как растворитель ацетилена в стальных баллонах. В номерные растворители ацетон добавляют для улучшения качеств растворения веществ и увеличения летучести растворителя. Также очень широко используется для обезжиривания поверхности перед покрасочными работами.
Краткие характеристики ацетона:
| Наименование | Показатель |
| Внешний вид: |
Бесцветная прозрачная
жидкость |
| Плотность ацетона при +20С, г/см3: | 0,789-0,791 |
| Молекулярная масса ацетона: | 58,08 |
| Предел температуры кипения (при 101,3 кПа), С: | 56,2 |
| Температура замерзания ацетона: | минус 95°С |
| Коэффициент преломления ацетона: | 1,359 |
| Вязкость ацетона при +20°С: | 0,33 мПа/сек |
| Давление насыщенного пара ацетона при +20°С: | 24,1 кПа |
| Температура вспышки ацетона: | минус 19°С |
| Температура самовоспламенения ацетона: | 500°С |
Внимание ацетон не растворяет!!! — Полиакрилонитрил, полиамиды и каучук.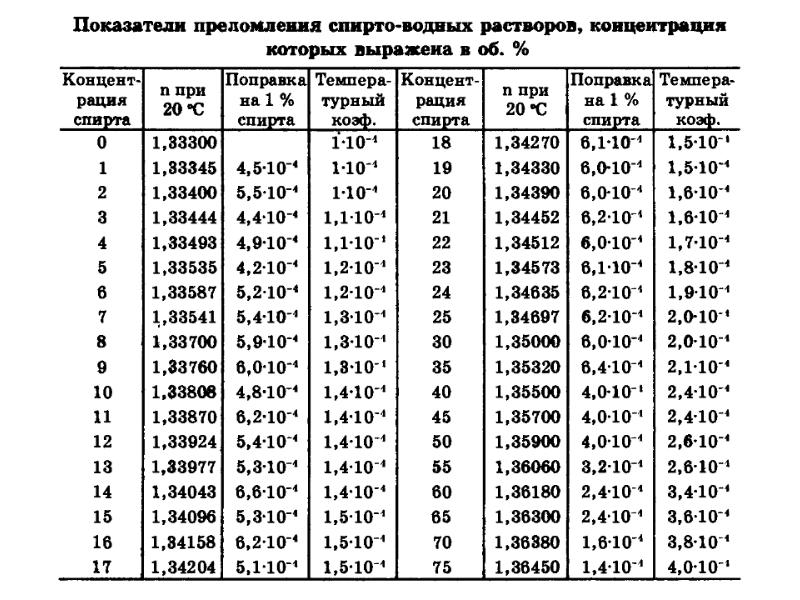
Ацетон хорошо растворяет: сложные и простые эфиры целюлозы, кетоновые смолы, кетон-формальдегидные смолы, полиакрилат, полистирол, полиамиды, жиры, природные и синтетические масла, хлоркаучук.
Требования безопасности и хранения:
- ацетон по степени воздействия на организм относится к 4 классу опасности — малоопасные вещества
- ацетон при высоких концентрациях действует наркотически. При попадании на кожу всасывается организмом.
- ацетон относится к легковоспламеняющимся продуктам: температура самовоспламенения 500 °С,
- Предельно допустимая концентрация паров ацетона в воздухе рабочей зоны составляет 200 мг/м3. При привышении указанной концентрации вероятно отравление!
- При работе с ацетоном необходимо применять индивидуальные средства защиты по типовым отраслевым нормам
-
При сливно-наливных операциях следует строго соблюдать правила защиты от статического электричества.
Всё оборудование и коммуникации должны быть защищены от статического электричества.
- Ацетон — Лекговоспламеняющаяся жидкость
- При вскрытии тары запрещается использовать инструмент дающий искру
- Запрещается слив и перекачка ацетона сжатым воздухом
- При сливе и перекачке ацетона необходимо соблюдать правила защиты от статического напряжения.
- Производственные и складские помещения, в которых ведутся работы с ацетоном, хранится ацетон должны быть обеспечены механической приточно-вытяжной вентиляцией, освещение и электрооборудование должно быть во взрывобезопасном исполнении
- В помещениях для хранения и применения ацетона запрещается обращение с открытым огнем, курение а также использование инструментов дающих искру (как электро так и ручного) .
- Внимание!!! ацетон при контакте с перекисью натрия или хромовым ангидридом — загорается со взрывом!
-
При розливе ацетона обезвреживание производить засыпкой песком с выносом его в специально отведенное место.
- Для тушения ацетона можно применять любые средства пожаротушения: вода, пена, порошковые огнетушители, углекислотные огнетушители, песок, асбестовое одеяло.
- Средства защиты органов дыхания в экстренной ситуации — противогаз марки «А» или «БКФ»
Гарантийный срок хранения ацетона:
- В металлической таре — 12 месяцев
- В стеклянной таре — 1 год
- В пластиковой таре — 1 месяц
Лабораторная работа №1
Тема: Изучение
равновесия жидкость-пар в двойных жидких
системах.
Цель:
1) Построение
фазовой диаграммы жидкость-пар в
координатах температура кипения-состав
системы.
2) Определение типа
двойной системы летучих жидкостей.
Для
работы готовят смеси толуола с ацетоном,
каждая смесь имеет объём 10 мл (см.
таблицу 2)
Таблица
2 – Опытные данные
|
Состав |
Показа-тель исходной смеси |
Температура |
Показа-тель конденсата (пара) |
Состав |
||||
|
ацетон |
толуол |
ацетон |
толуол |
|||||
|
объ-ёмные % |
V, мл |
объёмные % |
V, мл |
|||||
|
100 |
10 |
0 |
0 |
|||||
|
90 |
9 |
10 |
1 |
|||||
|
80 |
8 |
20 |
2 |
|||||
|
70 |
7 |
30 |
3 |
|||||
|
60 |
6 |
40 |
4 |
|||||
|
50 |
5 |
50 |
5 |
|||||
|
40 |
4 |
60 |
6 |
|||||
|
30 |
3 |
70 |
7 |
|||||
|
20 |
2 |
80 |
8 |
|||||
|
10 |
1 |
90 |
9 |
|||||
|
0 |
0 |
100 |
10 |
|||||
-показатель
преломления жидкости при 200
С.
Для
индивидуальных жидкостей (толуол,
ацетон) показатель преломления и
температура кипения являются справочными
величинами.
Смеси
толуола и ацетона готовят в сухих
пробирках. Толуол и ацетон отмеряют
пипетками. Пробирку со смесью закрывают
резиновой пробкой и перемешивают смесь,
переворачивая вверх-вниз дном. Толуол
растворяет резину и смесь может окраситься
в желтый цвет. Время контакта смеси с
пробкой должно быть минимальным,
перемешивание проводят быстро. Объем
ацетона и толуола в смесях может быть
изменен при необходимости (см. таблицу
2). Определяют показатель преломления
толуола, ацетона и сравнивают с табличными
величинами. Показатели преломления
смесей должны находиться в интервале
значений показателей преломления чистых
ацетона и толуола. На измерительную
призму рефрактометра наносят 3-4 капли
жидкости, жидкость удобно лить по
стеклянной палочке. Определение
показателей преломления следует
проводить быстро, так как ацетон и толуол
являются легко летучими жидкостями
(см.
работы на рефрактометре состав смесей
на поверхности призмы может измениться.
Значения показателей преломления чистых
жидкостей и исходных смесей заносят в
таблицу.
Определяют
температуру кипения чистых жидкостей
и их смесей. Схема прибора для определения
температуры кипения представлена на
рисунке 12.
1
— колба, в которую вливают исследуемую
жидкость; 2 — боковой отвод колбы; 3 — горло
колбы; 4 — термометр; 5 — пробка; 6 —
пробирка-приемник; 7 — исследуемая
жидкость
Рисунок
12 – Схема прибора для изучения равновесия
жидкость-пар в двойных системах
Прибор
закрепляют в лапках штатива. Нагрев
колбы с жидкостью осуществляют на
электроплитке. Всю смесь выливают в
колбу, лить следует по той части горла
колбы, где нет отверстия, чтобы смесь
не потекла в боковой отвод. В жидкость
помещают 2-3 “кипятильника” (кусочки
пористого фарфора). В колбу вставляют
термометр, который крепится на пробке.
Ртутный шарик термометра должен быть
погружён в жидкость.
жидкости судят по появлению пузырьков.
Температуру начала кипения записывают.
Отбирают в пробирку- приёмник около 0.5
мл смеси-конденсата. Первые 2-3 капли
конденсата можно отбросить, собрав их
в другую пробирку-приёмник. Записывают
температуру конца отбора пробы.
Температурой кипения раствора является
температура, средняя из двух: начало
закипания смеси и конец отбора
смеси-конденсата. Пробирку с конденсатом
закрывают пробкой, охлаждают под краном
при необходимости, определяют показатель
преломления конденсата и вносят эту
цифру в таблицу. После отбора конденсата
нагревание смеси прекращают, остаток
смеси выливают в специальный сосуд под
тягой. Смесь из колбы следует выливать
по той части горла колбы, где нет
отверстия, чтобы смесь не потекла в
боковой отвод. Ещё тёплую колбу высушивают,
для чего продувают её грушей под тягой
и делают опыт со смесью другого состава.
По
полученным в эксперименте данным строят
график зависимости
от состава исходных смесей (калибровочный
график).
бумаге. Обычно зависимость показателя
преломления от состава смесей является
линейной.
По
графику зависимости показателя
преломления исходных смесей от их
состава определяют состав пара
(конденсата), зная его показатель
преломления.
Зная
состав исходной жидкости в объёмных
процентах, её температуру кипения и
зная состав пара, строят фазовую диаграмму
жидкость-пар в координатах температура
кипения-состав (объёмные проценты),
По
виду диаграммы делают вывод о том, к
какому типу реальных растворов относится
смесь двух летучих жидкостей ацетон–толуол.
Реактивы
-
Ацетон.
-
Толуол.
Посуда
и приборы
-
Пипетки
на 10 мл – 2 шт. -
Пипетки
на 2 мл – 2 шт. -
Прибор
для определения температуры кипения
растворов. -
Электроплитка.
Контрольные
вопросы для защиты лабораторной работы.
1.
Фазовые равновесия. Общие понятия: фаза,
компонент, число независимых компонентов,
число термодинамических степеней
свободы.
2.
Общие термодинамические условия
равновесия в гетерогенных системах и
критерий направления процессов в
гетерогенных системах.
3.
Правило фаз Д.У. Гиббса, вывод.
4.
Классификация систем по числу фаз,
компонентов, по числу термодинамических
степеней свободы.
5.
Идеальные растворы, термодинамическая
характеристика.
6.
Закон Рауля, вывод. Закон Генри.
Объединенный закон Рауля – Генри.
7.
Фазовая диаграмма жидкость – пар для
идеальных растворов.
8.
Положительные и отрицательные отклонения
от закона Рауля.
9.
Реальные растворы с положительными и
отрицательными отклонениями от закона
Рауля без азеотропной смеси. Фазовые
диаграммы жидкость – пар в координатах
давление – состав, температура кипения
– состав.
числа термодинамических степеней
свободы в разных точках на диаграмме.
Первый закон Д. П. Коновалова.
10.
Реальные растворы с положительными и
отрицательными отклонениями от закона
Рауля с азеотропной смесью. Второй закон
Д. П. Коновалова, азеотропные смеси.
11.
Прикладное значение законов
Д. П. Коновалова. Перегонка и
ректификация
12.
Методы разделения азеотропных смесей.
Литература
-
Курс
физической химии / Под редакцией Я. И.
Герасимова. – М.:
Химия. Т.1. 1970. – С.174-186, 188-192.
2. Практикум по
физической химии / Под редакцией И. В.
Кудряшова. – М.: Высшая школа. 1986. –
С.191-202.
3.Физическая химия
/ Под редакцией К. С. Краснова. – М.: Высшая
школа. 1982. – С.338-345, 351-355, 361-364,
388-395.
4. Краткий
справочник физико-химических величин
/ Под редакцией А.
А. М. Пономаревой. – Л.: Химия, 1988. –
С.14, 16, 30.
5. Инструкция
по охране труда при проведении работ в
лаборатории кафедры химии №28. 2003.
Правила
по
технике
безопасности.
1.
При работе с органическими растворителями
следует помнить об их ядовитости и
высокой летучести. Работу с ними следует
проводить под тягой. При отмеривании
органических растворителей пипетками
втягивать растворитель в пипетку следует
резиновой грушей. Отработанные
органические растворители выливают в
специальный сосуд под тягой. Выливать
в раковину органические растворы
категорически воспрещается.
2.
Для предупреждения бурного вскипания
и выбрасывания жидкости необходимо
помещать в сосуд несколько капилляров,
один конец которых запаян, или кусочки
пористого фарфора (“кипятильники”).
“Кипятильники” следует вносить только
в холодную жидкость.
3.
При работе с ртутными термометрами
следует помнить о высокой ядовитости
ртути.
сообщить об этом преподавателю или
лаборанту. Разлитую ртуть собирают с
помощью амальгамированной медной
проволоки или вакуумной ловушки. Место,
где была разлита ртуть, тщательно
смазывают концентрированным раствором
хлорного железа (ІІІ) и оставляют на
сутки, затем моют, сушат, и, наконец,
засыпают мелким порошком серы.
4. Перед включением
электроприбора в сеть необходимо
проверить исправность заземления,
исправность изоляции всех токоведущих
частей прибора, правильность подключения
всех элементов схемы прибора.
5. При нарушении
изоляции и загорании электропроводов
следует немедленно отключить общее
напряжение и только после этого тушить
провода одеялом, огнетушителем или
другими средствами. Воспрещается тушение
проводов любыми способами до выключения
рубильника.
Ион Оксония
Ион Оксония
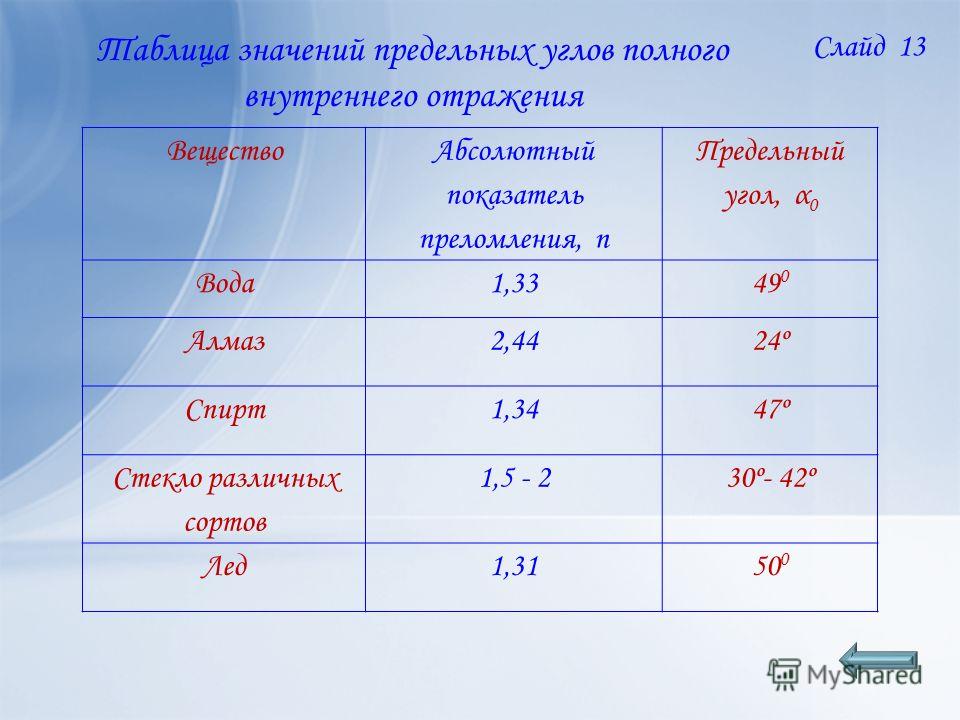
Показатель преломления
— это физическое свойство твердых и жидких тел. Легкие путешествия
через разные материалы под разными углами от входящего светового луча.
Например, свет распространяется в воздухе по прямой линии, но когда свет входит
другой материал, такой как кварцевая призма, свет преломляется в определенной
угол от угла, под которым свет движется, прежде чем он войдет в это вещество.
Преломление иногда называют «преломлением света», но это неверно.
термин, поскольку вы не преломляете свет, вы преломляете свет.
Ниже приведены некоторые репрезентативные значения показателя преломления для химических веществ, обычно
используется в лаборатории.
| Химическое название |
Показатель преломления (n Д ) |
|---|---|
| Трифторуксусная кислота | 1.2850 |
| Метанол | 1.3284 |
| Вода |
1.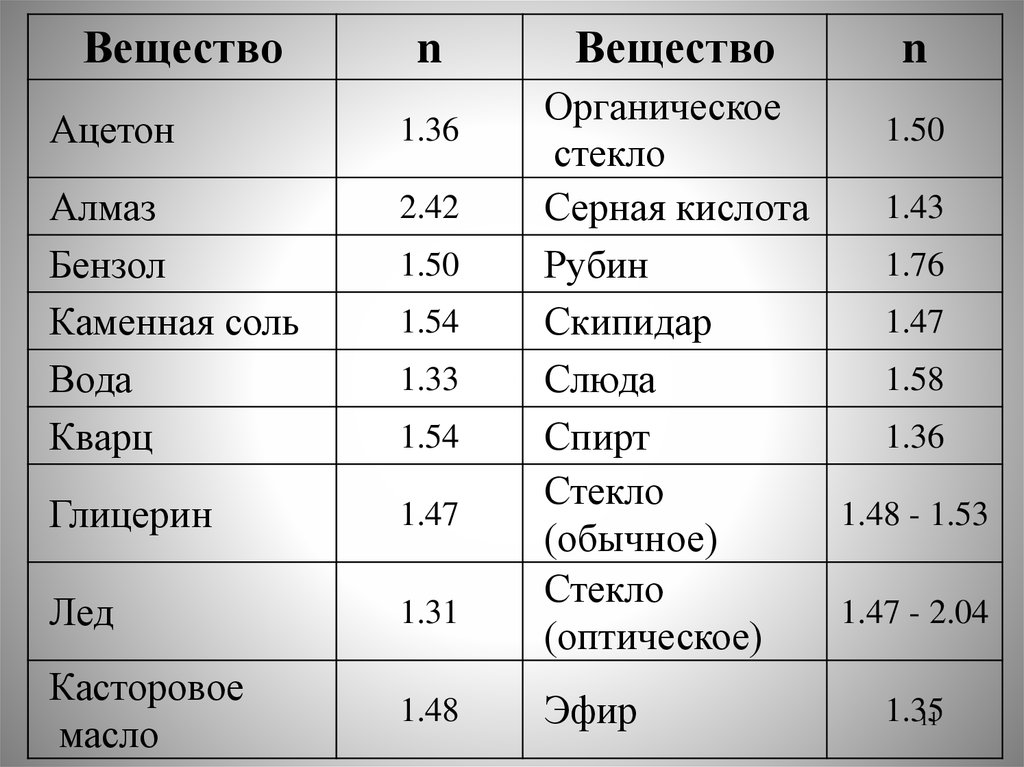 3330 3330 |
| Ацетонитрил | 1.3441 |
| Этиловый эфир | 1,3524 |
| 1,1,2-трихлортрифторэтан |
1,3557 (25С) |
| Пентан | 1,3575 |
| Ацетон | 1,3586 |
| Этиловый спирт | 1.3614 |
| Петролейный эфир | 1.3650 |
| Метил t -Бутиловый эфир | 1,3689 |
| Этилацетат | 1,3724 |
| Гексан | 1.3749 |
| Изопропиловый спирт | 1,3772 |
| Метилэтилкетон | 1,3788 |
| Глайм | 1,3796 |
| n -Пропиловый спирт | 1,3856 |
| Гептан | 1,3876 |
| Метил n -Пропилкетон |
1.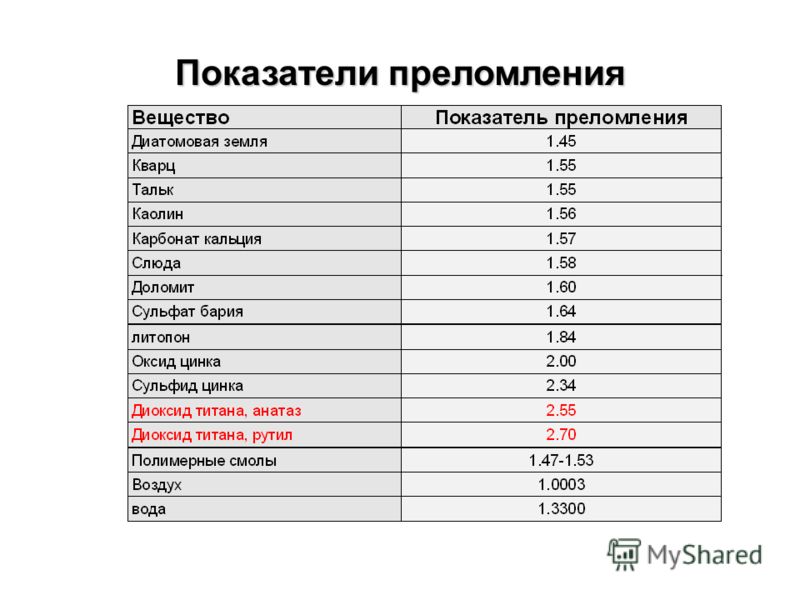 3901 3901 |
| Изооктан | 1,3914 |
| n — Бутилацетат | 1,3942 |
| Метилизобутилкетон | 1,3957 |
| Изобутиловый спирт | 1,3959 |
| n — Бутиловый спирт | 1,3993 |
| Триэтиламин | 1.4010 |
| n — Бутилхлорид | 1,4021 |
| 2-метоксиэтанол | 1.4021 |
| Циклопентан | 1.4064 |
| Метилизоамилкетон | 1.4070 |
| Тетрагидрофуран | 1.4072 |
| Пропиленкарбонат | 1.4210 |
| 1,4-диоксан | 1.4224 |
| Дихлорметан | 1.4241 |
| Циклогексан |
1.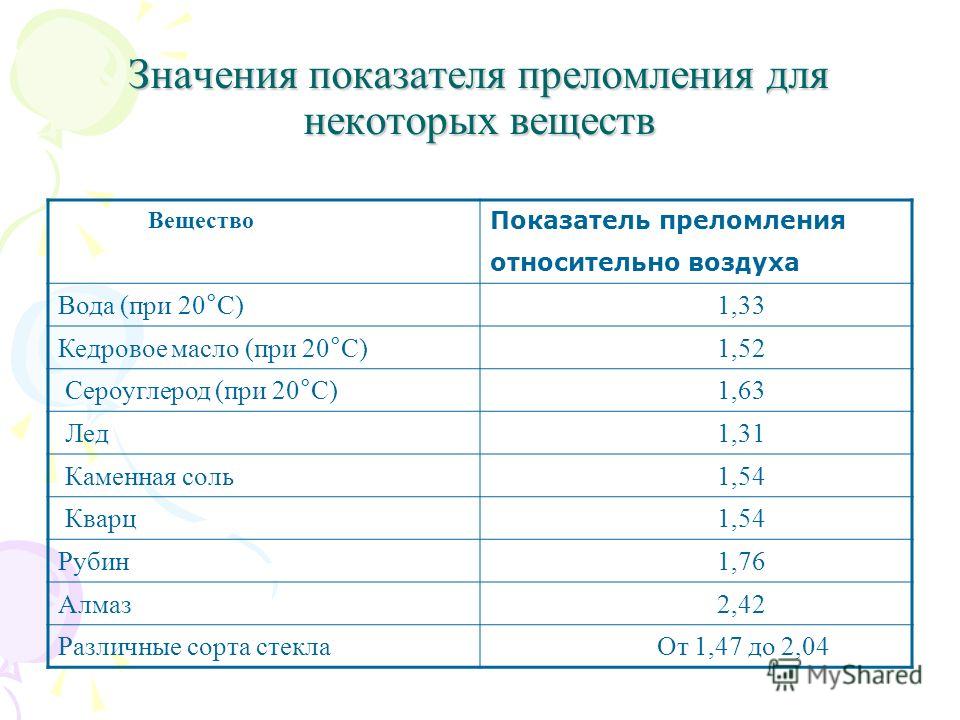 4262 4262 |
| N , N -Диметилформамид | 1.4305 |
| Изопропилмиристат | 1.4332 |
| Диметилацетамид | 1.4384 |
| Этилендихлорид | 1.4448 |
| Хлороформ | 1.4458 |
| N -Метилпирролидон | 1.4700 |
| Диметилсульфоксид | 1,4793 |
| Толуол | 1,4969 |
| o — Ксилол | 1,5054 |
| Пиридин | 1,5102 |
| Хлорбензол | 1,5248 |
| o — Дихлорбензол | 1.5514 |
| 1,2,4-трихлорбензол | 1,5717 |
Авторские права доктора Дональда Л.
06.10.2010)
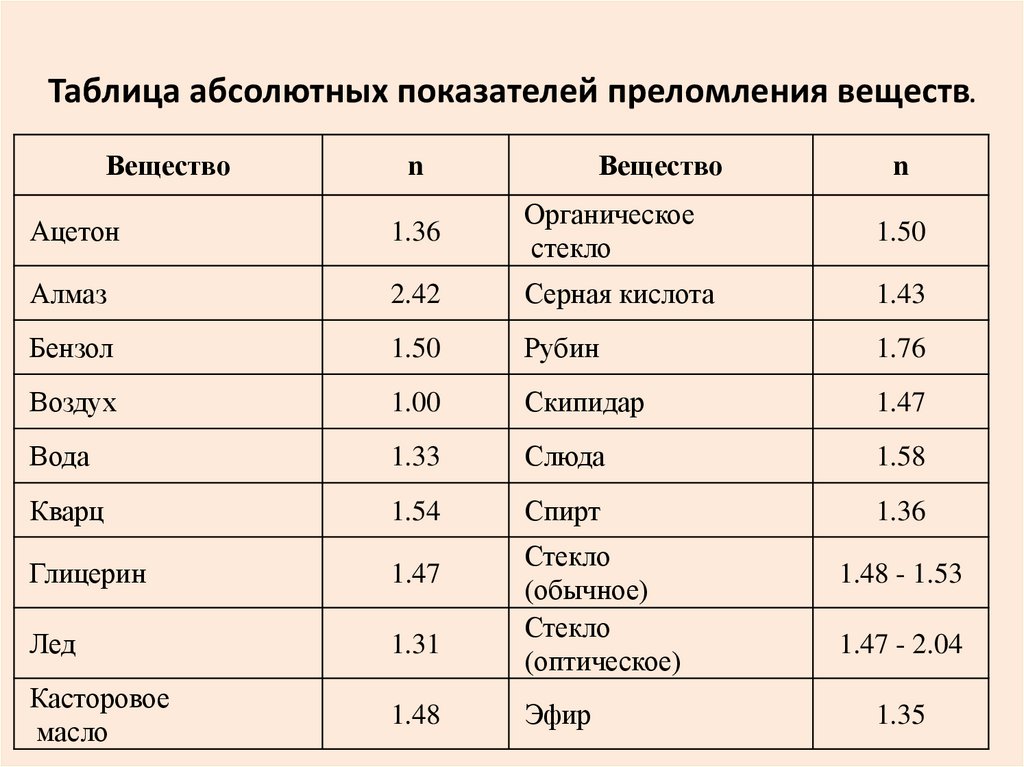
Показатель преломления общий Жидкости, твердые тела и газы
Преломление — это эффект, возникающий между прозрачными материалами различной плотности.
Показатель преломления — n — среды является мерой того, насколько уменьшается скорость света внутри среды. Скорость света в среде можно выразить как
v = c / n (1)
где
v = скорость света в среде
400
c = скорость света в воздухе или вакуум — примерно 3 10 8 м/с (или 299792458 м/с)
n = показатель преломления
Показатель преломления определяется как
7 90 скорость света в вакууме по скорости света в среде».
Экв. 1 модифицированный
n = c / v
09 019 8 Бром 8 Гелий
19 019 8 1 0009 900 9 0 9 0 1 9 0 1 9 0 9 0 1 9 0 0018 Хлороформ
9 8 Хладагент дихлордифторметан R-12 М 90 этил салилат 0018 1,538
8 405
6 6 C 9 019
Показатели преломления некоторых распространенных газов
Газ
Показатель преломления
— n —
Ацетон
1.

Воздух (-15 o C)
19
1942
Воздух (0 или Ц)
1.00029238
Воздух (15 или Ц) 9 70
1.100018 1.000919 70
1.00018 0016
Воздух (30 или С)
1.00026337
Воздух (60 o C)
1.00023958
Спирт этиловый
1.000878
0 Спирт метиловый
Аммиак
1.000376
Аргон
1.000281
Бензол
1.001762
0019
Двуокись углерода
1.000449
Сероуглерод
1.001481
Окись углерода 900 1.000338
Хлор
1.000773
Хлороформ
1.001450
Эфир этиловый
1.001533
Эфир метиловый
1.
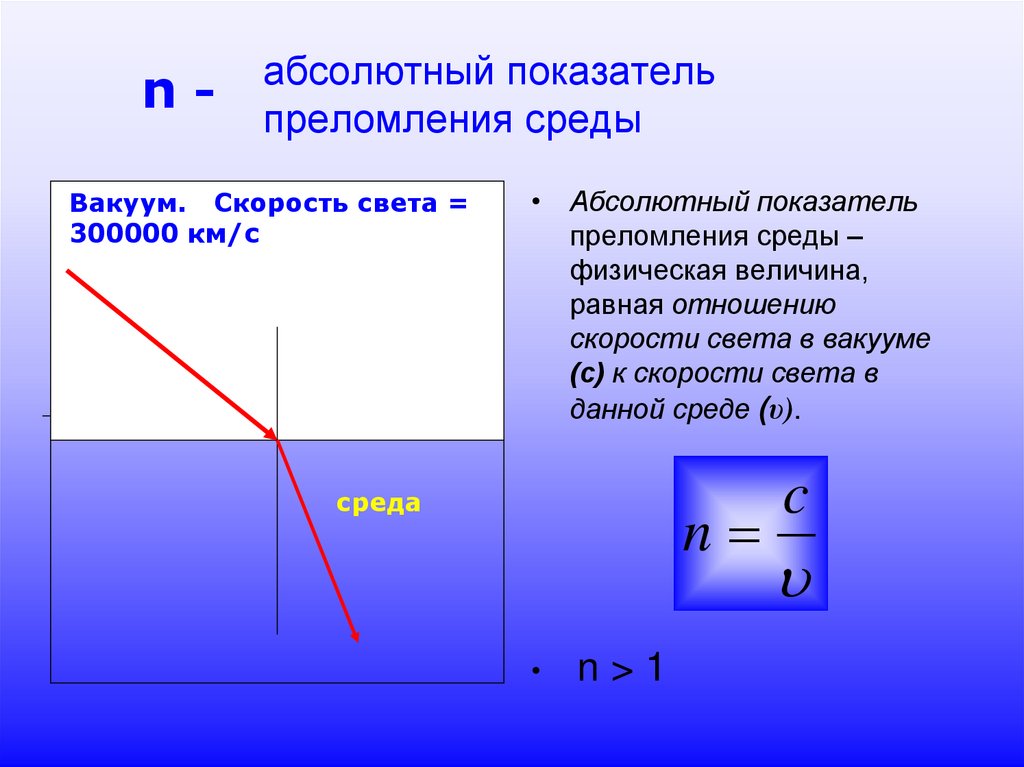
Соляная кислота
1.000447
Водород
1.000132
Метан
1.000444
Оксид азота
1.000297
Азот
1.000298
Закись азота
1.000516
Кислород
1.000271
Пентан
9 9.00189 19
Диоксид серы
1.000686
Водяной пар
1.000261
Показатель преломления для обычных жидкостей
Жидкость
Показатель преломления
— n —
Уксусная кислота
1,37
Ацетон
1,36
Спирт этиловый (этанол) 9 0
Спирт метиловый (метанол)
1,33
Спирт пропиловый
1.
Анилин
1.586
Бензол
1.501
9
Бензол 1,568
Сероуглерод
1,63
Четыреххлористый углерод
1,46
Хлорбензол
1,44
Декан
1,41
Додекан
1,41
Эфир
1,35
Этиленгликоль
1,43
Этилсалицилат
1,523
Этилциннамат
1,559
Трихлорфторметановый хладагент R-11
1,37
1,29
Хладагент хлордифторметан R-22
1,26
Фуран
1,47
Глизерин (Глицерин)
1,47
Гептан
1.38
Гексан
1.

Водород жидкий
1.0974
Метилен-йод
1,737
Молоко
1,35
Октан
1,40
Масло кедровое
1,516
Масло растительное 50 или C
1.47
Масло оливковое
1.46
Масло скипидарное
1.47
1.8 Альдегид 1.18
Парафин жидкий
1,48
Пропан
1,34
Пропилен
1.36
Пропиленгликоль
1.43
Хинолин
1.6199
Толуол
1.497
Скипидар (древесный)
1.47
Вода 0 o
Вода 20 или C
1.33283
Вода 100 o C
1,31766
Пример.
 Всё оборудование и коммуникации должны быть защищены от статического электричества.
Всё оборудование и коммуникации должны быть защищены от статического электричества.


Добавить комментарий