Содержание
Донорно-акцепторная связь
Донорно-акцепторная связь
Донорно-акцепторная связь
Ковалентная связь, образующаяся по донорно-акцепторному механизму, то есть за счет пары электронов одного из атомов, называется дoнорно-акцeпторной.
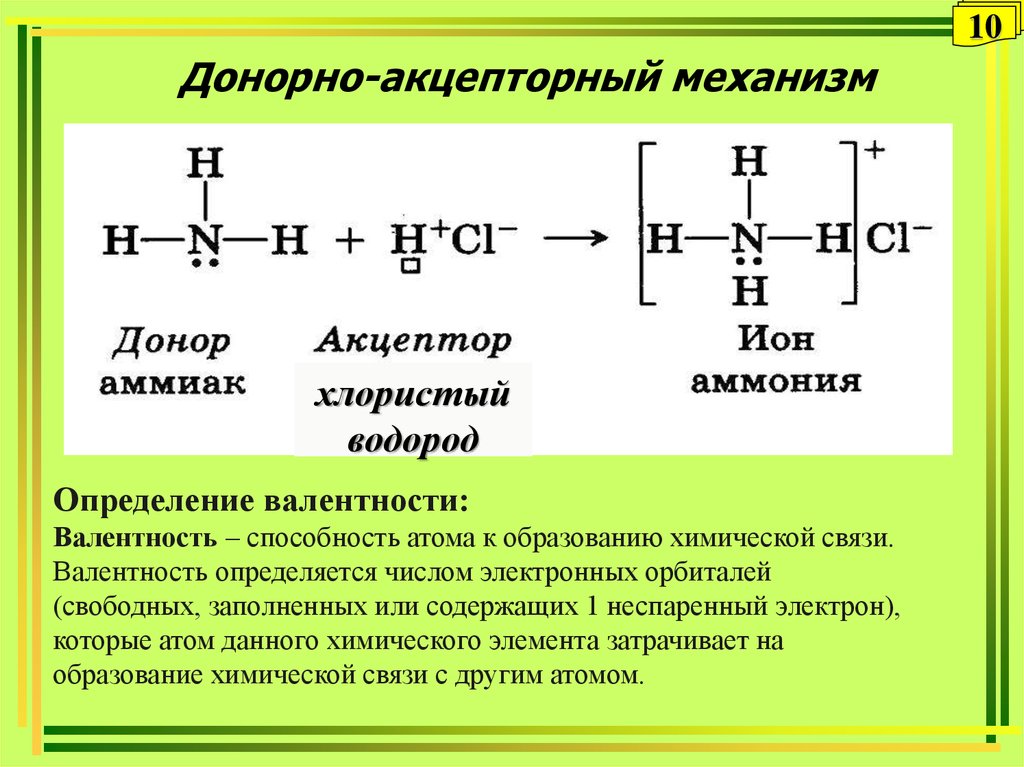
Например, такая связь образуется между атомом азота в молекуле метиламина CH3NH2 и протоном H+ кислоты HCl:
Атом азота отдает свою электронную пару для образования связи и выступает в роли донора, а протон H+ предоставляет вакантную орбиталь, играя роль акцептора. Атом-донор при этом приобретает положительный заряд.
Донорно-акцепторная связь отличается только способом образования; по свойствам она одинакова с другими ковалентными связями между аналогичными атомами.
Другой пример протонирование спиртов ROH при действии минеральных кислот, например, серной кислоты:
В этом случае донором является атом кислорода за счет одной из своих неподеленных электронных пар, а акцептором протон кислоты:
- Разновидностью донорно-акцепторной связи является семиполярная связь
Сeмипoлярная связь образуется при взаимодействии атома-донора пары электронов и атома-акцептора, не имеющих формальных зарядов.
При этом на атоме-доноре возникает положительный заряд, а на атоме-акцепторе, предоставившем вакантную орбиталь, – отрицательный.
Например, семиполярная связь O—Al образуется при реакции диметилового эфира (CH3)2O с хлоридом алюминия:Атом кислорода в молекуле диметилового эфира (CH3)2O отдает свою неподеленную пару электронов для образования связи с атомом алюминия, имеющим во внешнем слое только 6 электронов и готовым его дополнить до 8 в соответствии с правилом октета. В результате на атоме кислорода появляется положительный заряд, а на атоме алюминия – отрицательный. Противоположные по знаку заряды на ковалентно-связанных атомах вызывают их дополнительное электростатическое притяжение (ионную связь).
-
• Сочетание ковалентной и ионной связей называют сeмиполярной связью.
К семиполярным связям относится также связь азот-кислород в нитрогруппе NO2, входящей в состав азотной кислоты HO–NO2, ее солей и эфиров, а также нитросоединений R–NO2:
В приведенных формулах нитросоединения связи азота с кислородом неравноценны.
Однако, как показывают результаты физических исследований, эти связи энергетически совершенно одинаковы. Следовательно, электронная пара, обусловливающая отрицательный заряд, не сосредоточена целиком на каком-либо одном кислородном атоме, а несколько смещена к азоту при одновременном смещении от азота ко второму кислородному атому подвижной π-электронной пары двойной связи. В результате выравнивания электронной плотности в нитрогруппе формальный отрицательный заряд (-1) распределяется поровну (-1/2) между обоими атоми кислорода:
Решение
1.
Соединение «а»
+I-эффект
-I-эффект
-I-эффект
(донор) (акцептор)
(акцептор)
Так как в этом
соединении нет сопряжённой системы
связей, все имеющиеся здесь группы
проявляют только индуктивный эффект.
Карбонильная группа и атом хлора —
акцепторы электронной плотности, а СН3
-радикал – донор.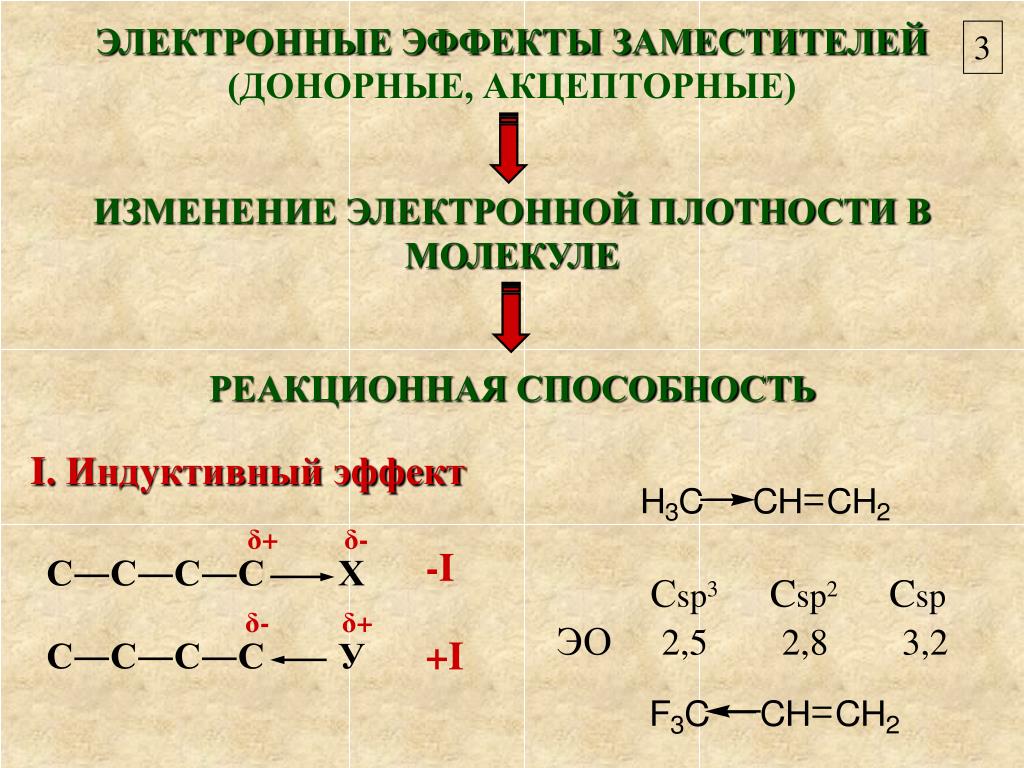
2.
Соединение «б»
-I-эффект,
-М-эффект
(акцептор).
В этом соединении
карбонильная группа является частью
сопряжённой системы. За счёт смещения
электронной плотности к атому кислорода
карбонильной группы, на атоме углерода
появляется некоторый недостаток
электронной плотности, поэтому
карбонильная группа смещает электронную
плотность на себя как по σ-связи
С1-С2
(-I-эффект),
так и по сопряжённой системе связей
(-М-эффект) и является акцептором
электронной плотности.
3.
Соединение «в».
-I,-М-
( акцептор ) — I,
+ М ( донор )
а) За счёт +I-эффекта
метильных групп увеличивается электронная
плотность на атоме азота. Неподелённая
пара электронов смещается в кольцо,
вступая в сопряжение с π-системой
кольца (+М-эффект). Поскольку азот имеет
большую величину электроотрицательности
чем углерод, электронная плотность
связи С—N смещена к атому азота (- I
-эффект).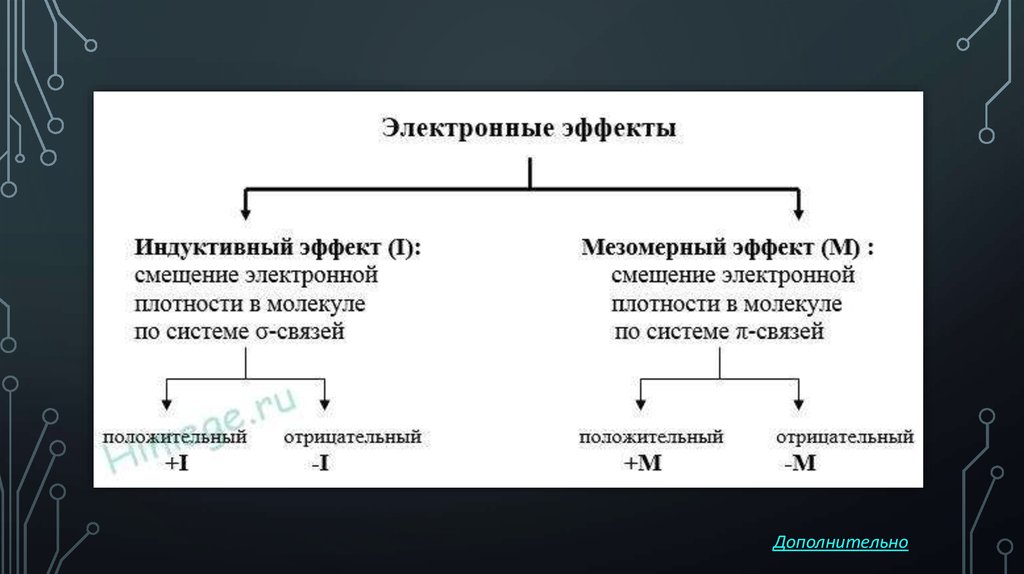
диметиламиногруппы больше — I
— эффекта, группа
является донором электронной плотности.
б) за счёт поляризации
двойной связи С=О карбоксильной группы
появляется некоторый положительный
заряд на атоме углерода. Поэтому
карбоксильная группа смещает электронную
плотность на себя как по σ-связи
(-I-эффект),
так и по сопряжённым связям (-М-эффект)
и является сильным акцептором.
4.Соединение
«г».
а).
Метильный радикал проявляет только
положительный индуктивный эффект,
смещая электронную плотность от себя
в кольцо (и является донором). У него
нет мезомерного эффекта, т.к. метильный
радикал не может стать частью сопряжённой
системы.
б).
Рассмотрим электронное влияние
гидроксильной группы. За счёт большей
электроотрицательности кислорода
одинарная связь С-ОН поляризована, и
электронная плотность смещена к атому
кислорода (-I
-эффект). Неподелённая пара электронов
атома кислорода является частью
сопряжённой системы и может оказывать
мезомерное влияние: эта пара электронов
смещается в сторону сопряжённой системы
кольца, и гидроксильная группа проявляет
+М-эффект.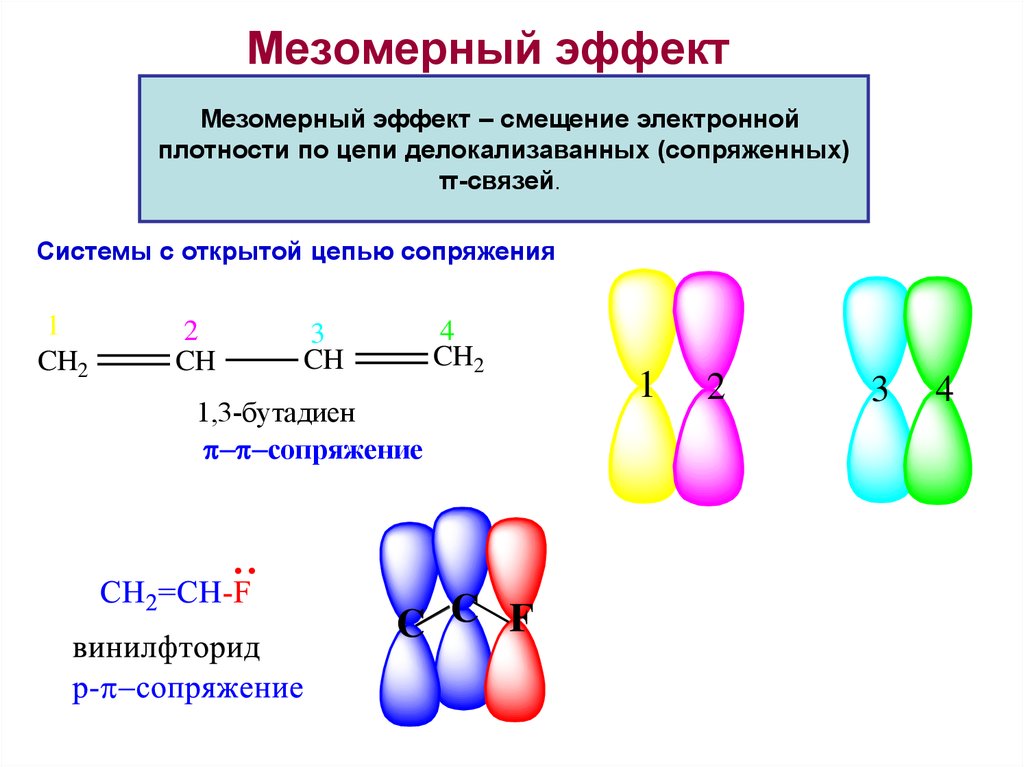
больше индуктивного, ОН-
группа является донором.
в) Нитрогруппа
входит в сопряжённую систему. За счёт
положительного заряда, имеющегося на
атоме азота, она вытягивает электронную
плотность на себя, проявляя –М — эффект,
и является акцептором электронной
плотности. Связь С-N
поляризована в сторону атома азота, и
нитрогруппа проявляет –I
— эффект.
5.
Соединение «д».
-I,
+М-эффект +I-эффект
-I-эффект
(донор)
(донор) (акцептор)
а) В аминогруппе
связь С—N
поляризована, и электронная плотность
смещена к атому азота за счёт большей
электроотрицательности азота по
сравнению с углеродом. Проявляется –I
-эффект аминогруппы.
Неподелённая
пара электронов атома азота, являясь
частью сопряжённой системы, смещается
в сторону этой системы, и амино-группа
проявляет +М-эффект.
сильнее I-эффекта,
аминогруппа является донором электронной
плотности.
б) Метильный
радикал не может вступить в сопряжение
с имеющимся фрагментом сопряжения,
т.к. не имеет ни кратных связей, ни
свободных р-электронов. Поэтому СН3
-радикал проявляет только +I-эффект
и является донором электронной плотности.
в) Карбонильная
группа отделена от сопряжённого
фрагмента двумя одинарными связями, и
поэтому мезомерного эффекта нет. За
счёт имеющегося на атоме углерода
карбонильной группы некоторого
положительного заряда связи С1
— С2
и С2
– С3
поляризованы в сторону карбонильной
группы. Следовательно, эта группа
проявляет –I
-эффект и является акцептором электронной
плотности.
5.4B: доноры и акцепторы электронов
-
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 8914
- Boundless (теперь LumenLearning)
- Boundless
Цели обучения
- Распознавать различные типы доноров и акцепторов электронов
У прокариот (бактерии и археи) есть несколько разных доноров электронов и несколько разных акцепторов электронов.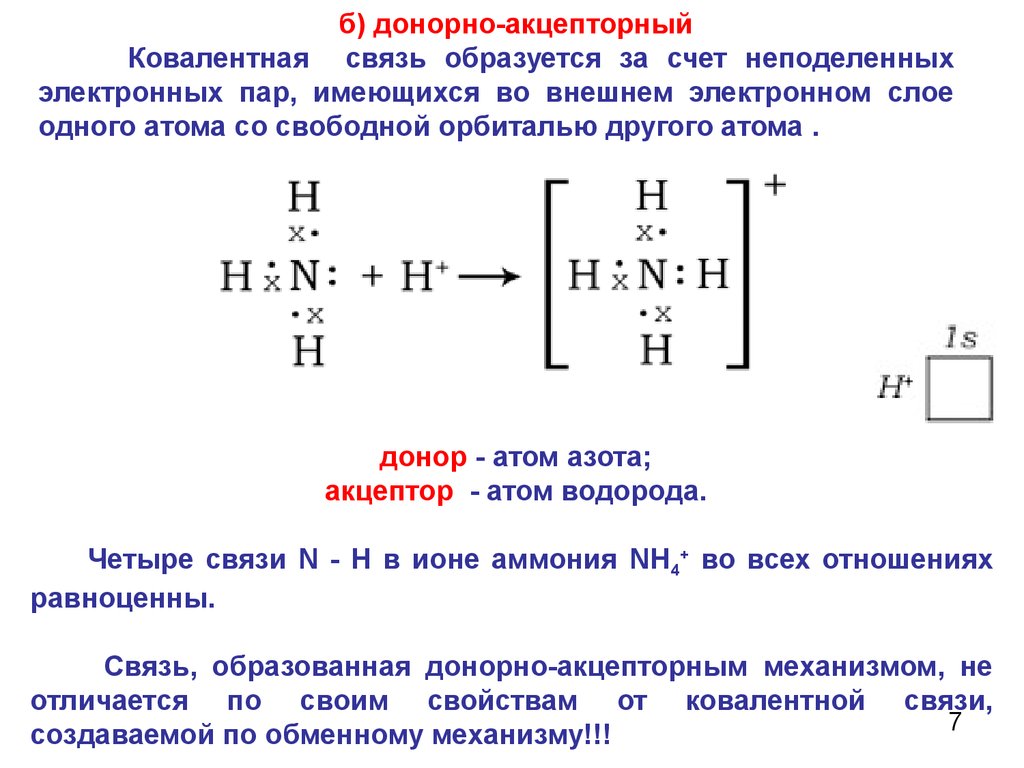
Рисунок: Обзор пути гликолиза : Обзор пути гликолиза. Этот путь, состоящий из серии реакций, производит много промежуточных продуктов и молекул, используемых в качестве субстратов для биосинтеза в дополнительных путях.
Отдельные бактерии используют несколько цепей переноса электронов, часто одновременно. Бактерии могут использовать ряд различных доноров электронов, ряд различных дегидрогеназ, ряд различных оксидаз и редуктаз и ряд различных акцепторов электронов.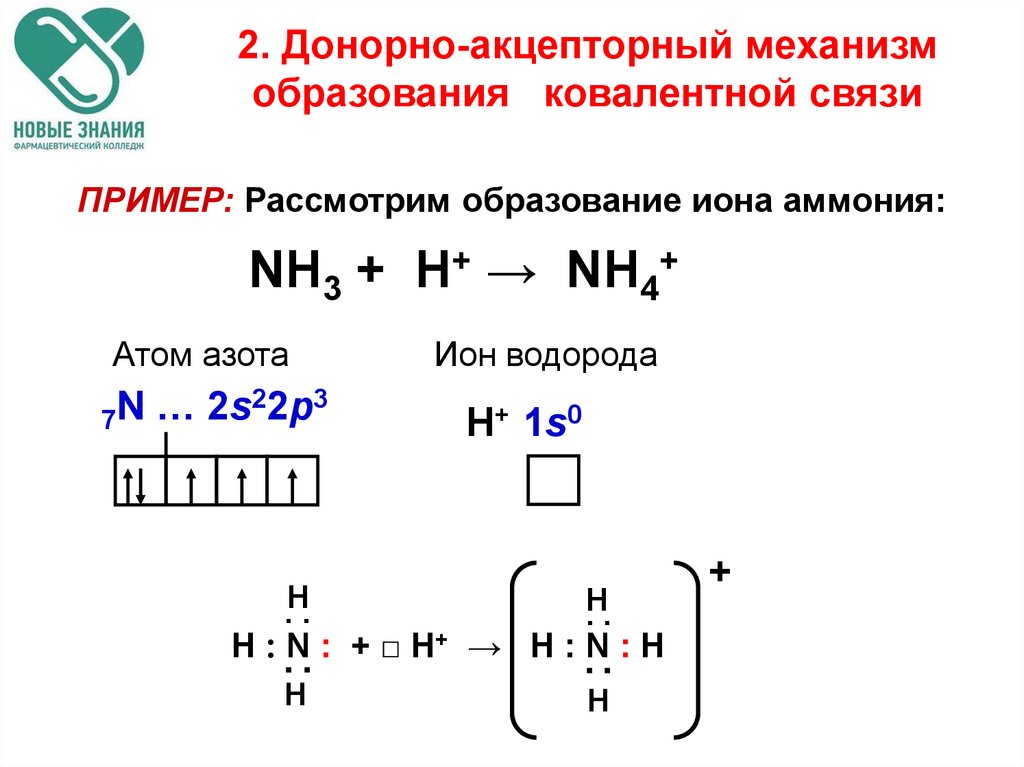
Общей чертой всех электронтранспортных цепей является наличие протонного насоса для создания трансмембранного протонного градиента. Бактериальные цепи переноса электронов могут содержать до трех протонных насосов, как митохондрии, или они могут содержать только один или два. Они всегда содержат по крайней мере один протонный насос.
В современной биосфере наиболее распространенными донорами электронов являются органические молекулы. Организмы, использующие органические молекулы в качестве источника энергии, называются органотрофами . Органотрофы (животные, грибы, протисты) и фототрофы (растения и водоросли) составляют подавляющее большинство всех известных форм жизни.
Некоторые прокариоты могут использовать неорганическое вещество в качестве источника энергии.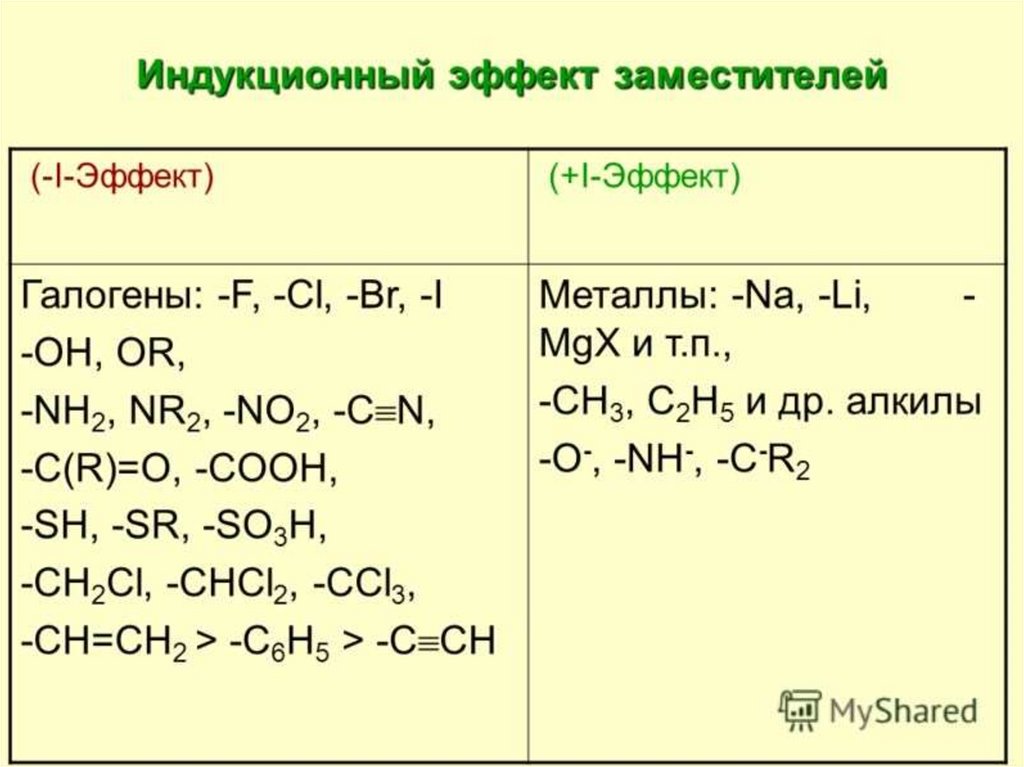
Использование неорганических доноров электронов в качестве источника энергии представляет особый интерес для изучения эволюции. Логически этот тип метаболизма должен был предшествовать использованию органических молекул в качестве источника энергии.
Так же, как существует ряд различных доноров электронов (органическое вещество у органотрофов, неорганическое вещество у литотрофов), существует множество различных акцепторов электронов, как органических, так и неорганических. Если кислород доступен, он неизменно используется в качестве конечного акцептора электронов, потому что он генерирует наибольшее изменение свободной энергии Гиббса и производит наибольшую энергию.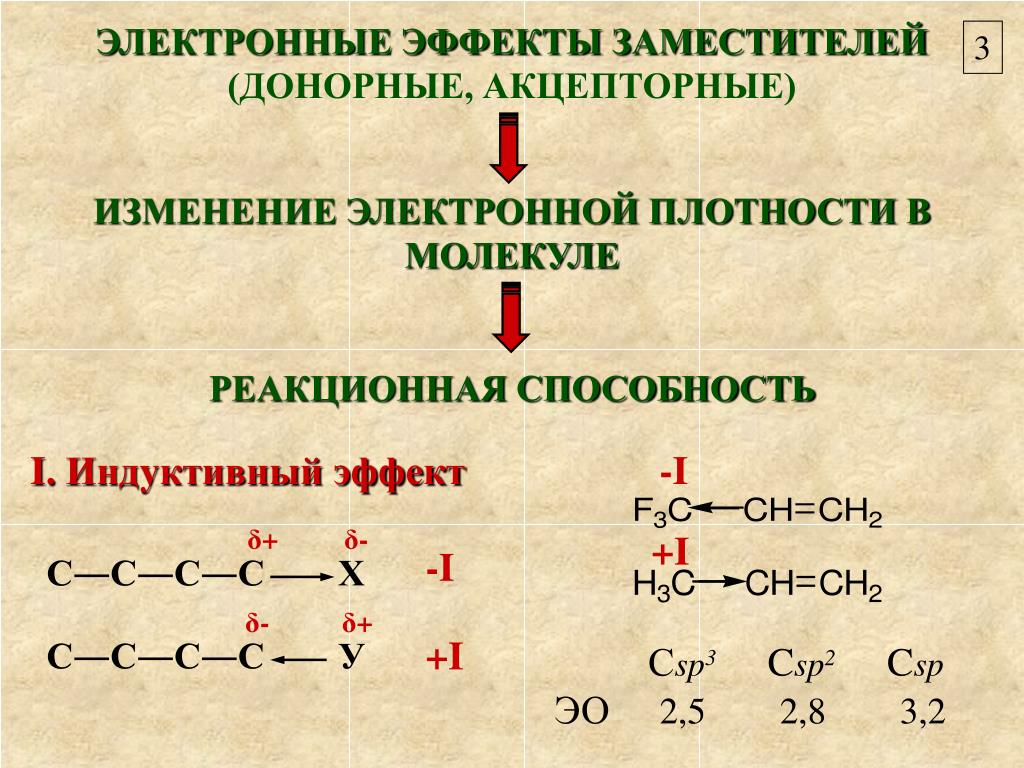
В анаэробной среде используются различные акцепторы электронов, включая нитраты, нитриты, трехвалентное железо, сульфаты, двуокись углерода и небольшие органические молекулы, такие как фумарат.
Поскольку цепи переноса электронов представляют собой окислительно-восстановительные процессы, их можно описать как сумму двух окислительно-восстановительных пар. Например, митохондриальная электрон-транспортная цепь может быть описана как сумма окислительно-восстановительной пары НАД + /НАДН и окислительно-восстановительной пары О 2 /Н 2 О. NADH является донором электронов, а O 2 — акцептор электронов.
Не каждая комбинация донор-акцептор термодинамически возможна. Окислительно-восстановительный потенциал акцептора должен быть более положительным, чем окислительно-восстановительный потенциал донора. Кроме того, фактические условия окружающей среды могут сильно отличаться от условий стандарта (1 молярная концентрация, парциальное давление 1 атм, pH = 7), которые применяются к окислительно-восстановительным потенциалам стандарта .
Бактериальные пути транспорта электронов, как правило, индуцируемы. В зависимости от окружающей среды бактерии могут синтезировать различные трансмембранные комплексы и продуцировать различные цепи переноса электронов в своих клеточных мембранах. Бактерии выбирают свои цепи переноса электронов из библиотеки ДНК, содержащей множество возможных дегидрогеназ, терминальных оксидаз и терминальных редуктаз. Ситуацию часто резюмируют, говоря, что цепи переноса электронов у бактерий разветвленный , модульный и индуцибельный .
Ключевые моменты
- Цепи переноса электронов бактерий могут содержать до трех протонных насосов.
- Наиболее распространенными донорами электронов являются органические молекулы.
- Существует ряд различных акцепторов электронов, как органических, так и неорганических. Если кислород доступен, он неизменно используется в качестве конечного акцептора электронов.
Ключевые термины
- органотроф : Организм, который получает энергию из органических соединений.
- литотроф : Организм, который получает энергию из неорганических соединений (таких как аммиак) посредством переноса электронов.
Эта страница под названием 5.4B: доноры и акцепторы электронов распространяется под лицензией CC BY-SA 4.0 и была создана, изменена и/или курирована Boundless.
- Наверх
-
- Была ли эта статья полезной?
-
- Тип изделия
- Раздел или Страница
- Автор
- Безграничный
- Лицензия
- CC BY-SA
- Версия лицензии
- 4,0
- Показать оглавление
- нет
-
- Теги
-
- литотроф
- органотроф
Электронодонорно-акцепторная способность отдельных лекарственных средств против COVID-19
1.
2. Ферри Г., Джуджиоли Д., Раймондо В., Л’Андолина М., Тавони А., Чекетти Р., Гвидуччи С., Урсини Ф., Каминити М., Варкасия Г. и др. COVID-19 и ревматические аутоиммунные системные заболевания: отчет о большой серии итальянских пациентов. клин. Ревматол. 2020;39:3195–3204. doi: 10.1007/s10067-020-05334-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Сюй Дж., Ши П.Ю., Ли Х., Чжоу Дж. Противовирусный агент широкого спектра действия никлозамид и его терапевтический потенциал. Заражение АКС. Дис. 2020;6:909–915. doi: 10.1021/acsinfecdis.0c00052. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Мурдака Г., Пьоджа Г., Негрини С. Витамин D и Covid-19: обновленная информация о доказательствах и потенциальных терапевтических последствиях. клин. Мол. Аллергия. 2020;18:1–8. doi: 10.1186/s12948-020-00139-0.
5. Warhurst D.C., Steele J.C.P., Adagu I.S., Craig J.C., Cullander C. Гидроксихлорохин гораздо менее активен, чем хлорохин, против резистентных к хлорохину Plasmodium falciparum , в соответствии с его физико-химическими свойствами. Дж. Антимикроб. Чемотер. 2003; 52: 188–193. doi: 10.1093/jac/dkg319. [PubMed] [CrossRef] [Google Scholar]
6. Такконе Ф.С., Горхэм Дж., Винсент Дж.Л. Гидроксихлорохин в лечении тяжелобольных пациентов с COVID-19: потребность в доказательной базе. Ланцет Респир. Мед. 2020; 8: 539–541. doi: 10.1016/S2213-2600(20)30172-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
7. Бенджамин Н., доктор медицины Рим, доктор медицины Джерри Эйворн Оценка лекарств во время Covid-19Пандемия. Н. англ. Дж. Мед. 2020; 382: 2282–2284. [PubMed] [Google Scholar]
8. Gautret P., Lagier J.C., Parola P., Hoang V.T., Meddeb L., Mailhe M., Doudier B., Courjon J., Giordanengo V.
9. Gautret P., Lagier J.C., Parola P., Hoang V.T., Meddeb L., Sevester J., Mailhe M., Doudier B., Aubry К., Амране С. и соавт. Клинический и микробиологический эффект комбинации гидроксихлорохина и азитромицина у 80 пациентов с COVID-19пациенты с последующим наблюдением не менее шести дней: пилотное обсервационное исследование. Путешествовать. Мед. Заразить. Дис. 2020;34:101663. doi: 10.1016/j.tmaid.2020.101663. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10. Lhazzani W., Møller M.H., Arabi Y.M. Кампания по выживанию при сепсисе: руководство по ведению взрослых в критическом состоянии с коронавирусной болезнью 2019 (COVID-19) Intensive Care Med. 2020; 46: 854–887.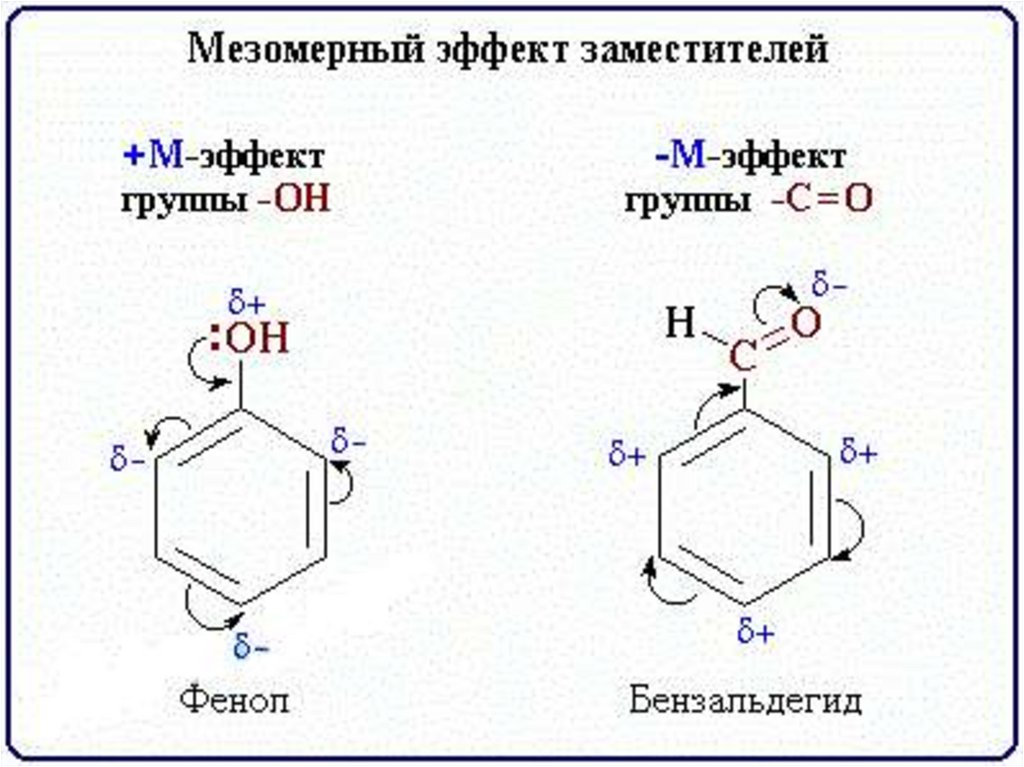
11. Хой С.М. Тройная комбинированная терапия карфилзомибом: обзор рецидивирующей множественной миеломы. Цель. Онкол. 2016; 11: 255–262. doi: 10.1007/s11523-016-0428-7. [PubMed] [CrossRef] [Google Scholar]
12. Мартинес А. Хлорохин и гидроксихлорохин: Инь-ян этих препаратов из теоретического исследования. Дж. Мекс. хим. соц. 2020;64:230–237. doi: 10.29356/jmcs.v64i3.1213. [CrossRef] [Google Scholar]
13. Ван Дж. Быстрая идентификация возможного медикаментозного лечения коронавирусной болезни-19(COVID-19) с помощью компьютерного исследования перепрофилирования лекарств. Дж. Хим. Инф. Модель. 2020;60:3277–3286. doi: 10.1021/acs.jcim.0c00179. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Suhail S., Zajac J., Fossum C., Lowater H., McCracken C., Severson N., Laatsch B., Narkiewicz-Jodko А., Джонсон Б., Либау Дж. и др. Роль окислительного стресса в инфекции SARS-CoV (SARS) и SARS-CoV-2 (COVID-19): обзор.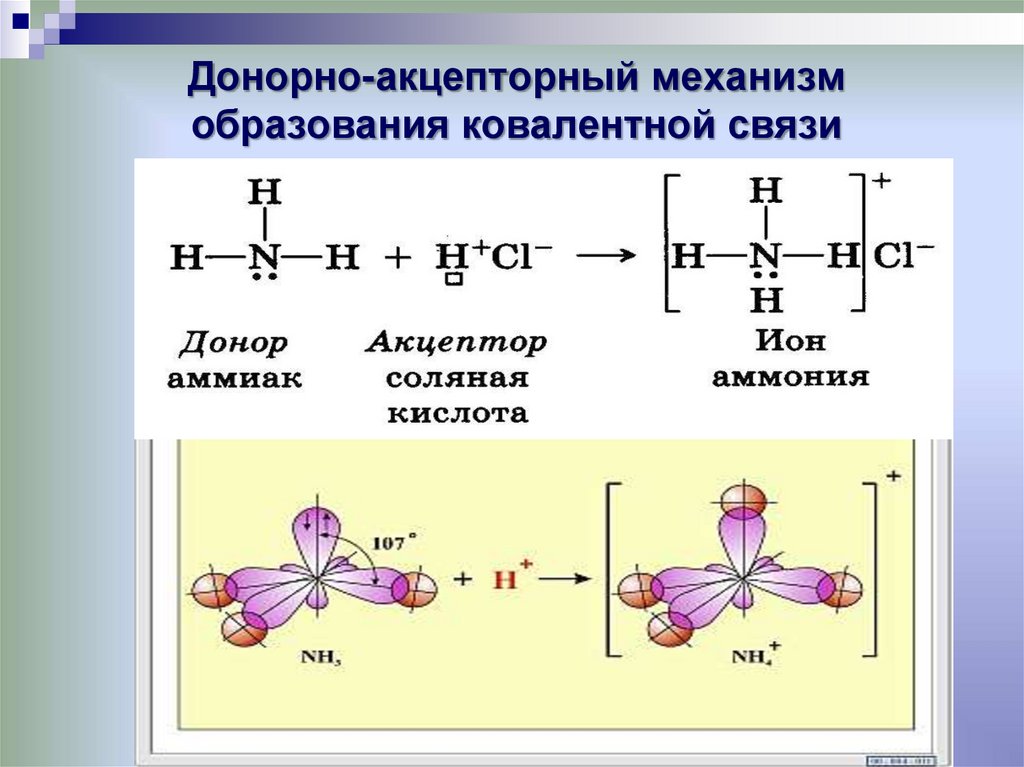
15. Хагар М., Ахмед Х.А., Алджохани Г., Альхаддад О.А. Исследование некоторых противовирусных N-гетероциклов в качестве лекарства от COVID 19: молекулярная стыковка и расчеты DFT. Междунар. Дж. Мол. науч. 2020;21:3922. doi: 10.3390/ijms21113922. [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Эльфикий А.А. Рибавирин, ремдесивир, софосбувир, галидесивир и тенофовир против РНК-зависимой РНК-полимеразы SARSCoV-2 (RdRp): исследование молекулярного докинга. Жизнь наук. 2020;253:117592. doi: 10.1016/j.lfs.2020.117592. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Kory P., Meduri U., Iglesias J., Varon J., Berkowitz K., Kornfeld H., Vinjevoll E., Mitchell С., Вагшул Ф., Марик П.Е. Обзор новых данных, демонстрирующих эффективность ивермектина в профилактике и лечении COVID-19. [(по состоянию на 12 мая 2021 г.
18. Ягисава М., Фостер П.Дж., Ханаки Х., Омура С. Глобальные тенденции клинических исследований ивермектина при COVID-19. Япония. Дж. Антибиот. 2021; 74: 44–95. [Google Scholar]
19. Мудацир М., Юфика А., Наину Ф., Фредиансях А., Мегавати Д., Праната А., Махдани В., Иксан И., Дхама К., Харапан Х. противовирусные активность ивермектина против sars-cov-2: старомодная собака с новым трюком. Обзор литературы. науч. фарм. 2020;88:36. doi: 10.3390/scipharm88030036. [CrossRef] [Google Scholar]
20. Olliaro P., Nevill C., LeBras J., Ringwald P., Mussano P., Garner P., Brasseur P. Систематический обзор лечения амодиахином неосложненной малярии. Ланцет. 1996;348:1196–1201. doi: 10.1016/S0140-6736(96)06217-4. [PubMed] [CrossRef] [Google Scholar]
21. Wu C., Liu Y., Yang Y., Zhang P., Zhong W., Wang Y., Wang Q., Xu Y., Li M., Ли Х. и др. Анализ терапевтических мишеней для SARS-CoV-2 и открытие потенциальных лекарств вычислительными методами.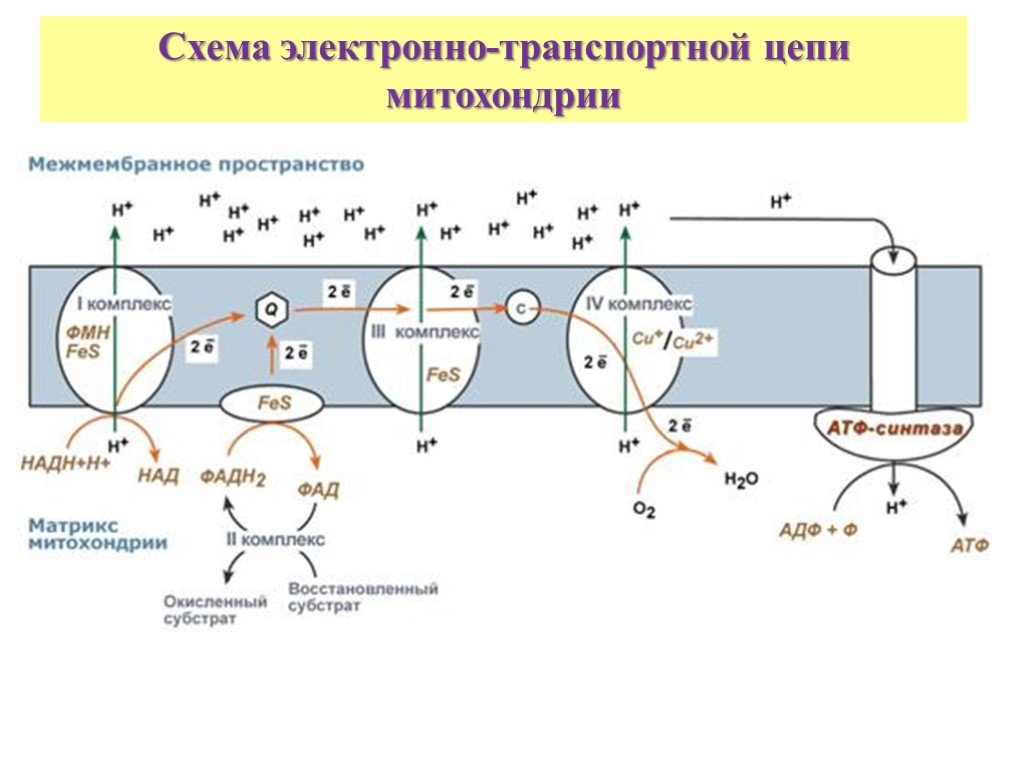
22. Hajialyani M., Farzaei M.H., Echeverría J., Nabav S.M., Uriarte E., Sobarzo-Sánchez E. Гесперидин как нейропротектор: обзор животных и клинических данных. Молекулы. 2019;24:648. doi: 10,3390/молекулы24030648. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Hwang S.L., Shih P.H., Yen G.C. Нейропротекторные эффекты цитрусовых флавоноидов. Дж. Агрик. Пищевая хим. 2012;60:877–885. doi: 10.1021/jf204452y. [PubMed] [CrossRef] [Google Scholar]
24. Тамбурин С., Мантовани Э., Де Бернардис Э., Зипето Д., Лугобони Ф. COVID-19 и связанные с ним симптомы у пациентов, принимающих дисульфирам при алкогольном расстройстве. Стажер Эмердж. Мед. 2021 г.: 10.1007/s11739-021-02633-у. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Юн Дж., Ким Г., Джархад Д.Б., Ким Х.Р., Шин Ю.С., Цюй С., Саху П.К., Ким Х.О., Ли Х.
26. Роберт М., Кокс Р.М., Вольф Дж.Д., Племпер Р.К. Терапевтически вводимый аналог рибонуклеозида MK-4482/EIDD-2801 блокирует передачу SARS-CoV-2 у хорьков. Нац. микробиол. 2021; 6:11–18. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E., Robb M.A., Cheeseman J.R., Montgomery J.J.A., Vreven T., Kudin K.N., Burant J.C., et al. Gaussian 09. Gaussian, Inc.; Уоллингфорд, Коннектикут, США: 2009 г. Редакция A.08. [Google Scholar]
28. Чжао Ю., Трухлар Д.Г. Набор функционалов плотности M06 для термохимии основной группы, термохимической кинетики, нековалентных взаимодействий, возбужденных состояний и переходных элементов: два новых функционала и систематическое тестирование четырех функционалов класса M06 и 12 других функционалов.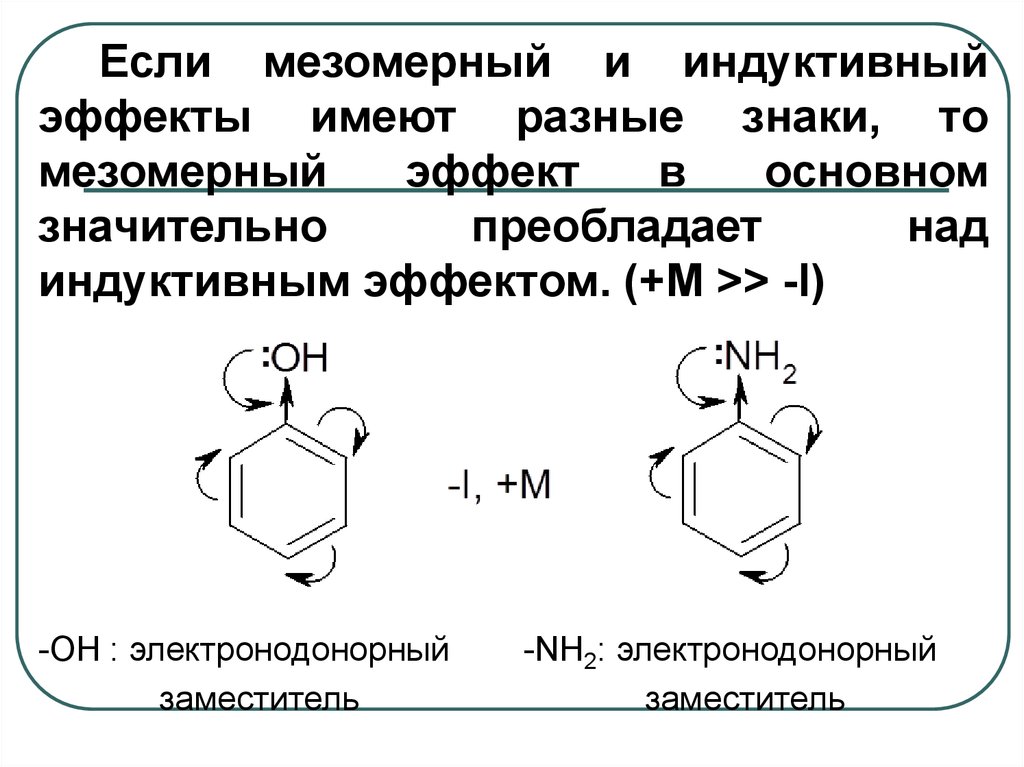
29. Петерссон Г.А., Беннетт А., Тенсфельдт Т.Г., Аль-Лахам М.А., Ширли В.А., Манцарис Дж.А. Полный базовый набор модельной химии. I. Полные энергии атомов с замкнутыми оболочками и гидридов элементов первого ряда. Дж. Хим. физ. 1988; 89: 2193–2218. doi: 10.1063/1.455064. [CrossRef] [Google Scholar]
30. Петерссон Г.А., Аль-Лахам М.А. Химия модели полного базового набора. II. Системы с открытой оболочкой и полные энергии атомов первого ряда. Дж. Хим. физ. 1991; 94: 6081–6090. дои: 10.1063/1.460447. [Перекрестная ссылка] [Академия Google]
31. Маклин А.Д., Чендлер Г.С. Сокращенные гауссовы базисы для молекулярных расчетов. I. Атомы второго ряда, Z = 11–18. Дж. Хим. физ. 1980; 72: 5639–5648. дои: 10.1063/1.438980. [CrossRef] [Google Scholar]
32. Кришнан Р., Бинкли Дж.С., Сигер Р., Попл Дж. Самосогласованные молекулярные орбитальные методы. ХХ. Базисный набор для коррелированных волновых функций. Дж. Хим.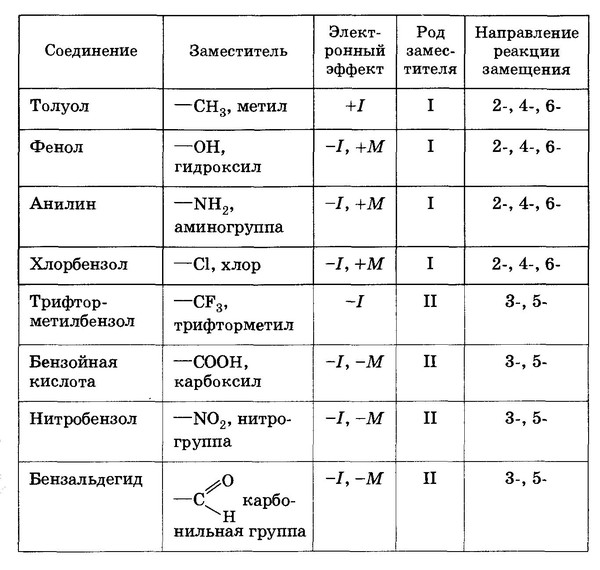
33. Geerlings P., Chattaraj P.K., De Proft F., Gázquez J.L., Liu S., Morell C., Toro-Labbé A., Vela A., Ayers P. Концептуальный функционал плотности теория: Состояние, перспективы, проблемы. Теор. хим. Акк. 2020;139: 5–18. doi: 10.1007/s00214-020-2546-7. [CrossRef] [Google Scholar]
34. Герлингс П., Де Профт Ф., Лангенакер В. Концептуальная функциональная теория плотности. хим. 2003; 103:1793–1874. doi: 10.1021/cr9
p. [PubMed] [CrossRef] [Google Scholar]
35. Черметт Х. Индексы химической активности в теории функционала плотности. Дж. Вычисл. хим. 1999; 20: 129–154. doi: 10.1002/(SICI)1096-987X(199
)20:1<129::AID-JCC13>3.0.CO;2-A. [CrossRef] [Google Scholar]
36. Лю С.Б. Концептуальная плотность Функциональная теория и некоторые последние разработки. Акта физ. хим. Грех. 2009 г.;25:590–600. [Google Scholar]
37. Ван Б., Ронг С., Чаттарадж П.К., Лю С. Сравнительное исследование для прогнозирования региоселективности, электрофильности и нуклеофильности с помощью функции Фукуи и заряда Хиршфельда.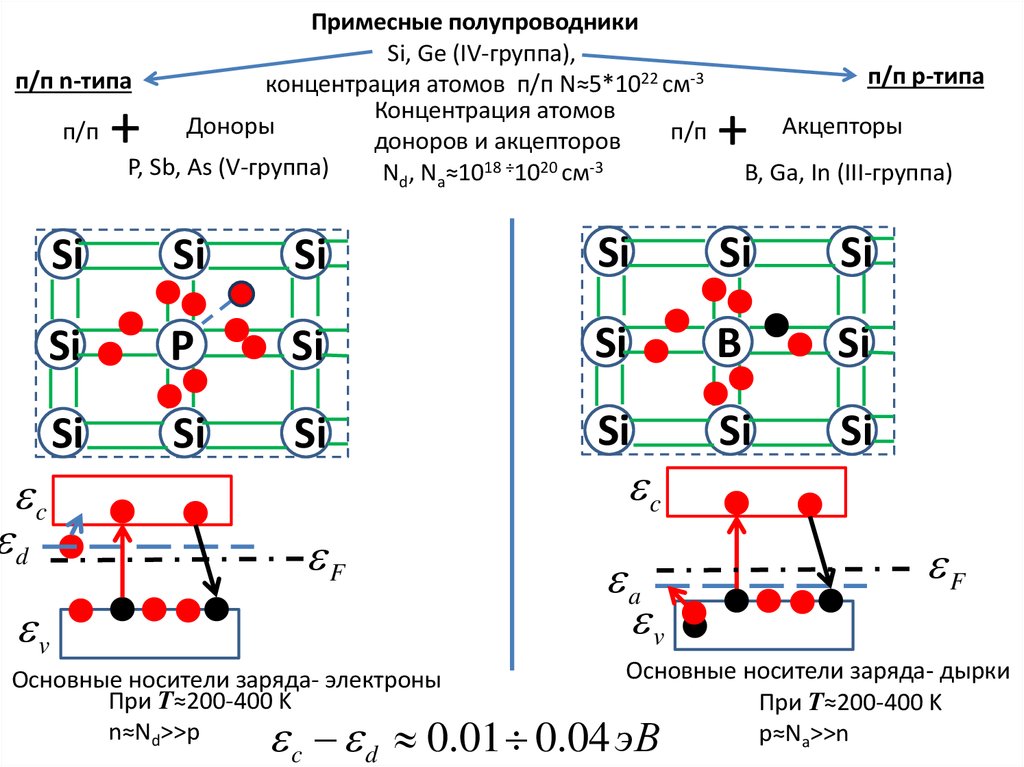
38. Газкес Х.Л., Седильо А., Вела А. Электродонация и электроакцепция. Дж. Физ. хим. А. 2007; 111:1966–1970. doi: 10.1021/jp065459f. [PubMed] [CrossRef] [Академия Google]
39. Газкес Х.Л. Перспективы теории функционала плотности химической реактивности. Дж. Мекс. хим. соц. 2008; 52:3–10. [Google Scholar]
40. Мартинес А., Родригес-Хиронес М.А., Барбоза А., Костас М. Карта донорных акцепторов каротиноидов, мелатонина и витаминов. Дж. Физ. хим. А. 2008; 112:9037–9042. doi: 10.1021/jp803218e. [PubMed] [CrossRef] [Google Scholar]
41. Мартинес А. Донаторная акцепторная карта пситтакофульвинов и антоцианов: являются ли они хорошими антиоксидантными веществами? Дж. Физ. хим. Б. 2009 г.;113:4915–4921. doi: 10.1021/jp8102436. [PubMed] [CrossRef] [Google Scholar]
42. Goode-Romero G., Winnberg U., Dominguez L., Ibarra I.A., Vargas R., Winnberg E., Martinez A. Новая информация о дофаминергических агентах на основе квантовых химические расчеты.
43. Goode-Romero G., Dominguez L., Vargas R., Ibarra I.A., Martinez A. Анализ энергии взаимодействия между дофаминергическими агентами и DRD2: Is Есть ли разница между рисперидоном (антагонист), арипипразолом (частичный агонист) и прамипексолом (агонист)? Комп. Теор. хим. 2021;1197:113125. doi: 10.1016/j.comptc.2020.113125. [CrossRef] [Google Scholar]
44. Cerón-Carrasco J.P., Bastida A., Requena A., Zuñiga J., Miguel B. Исследование теории функционала плотности стабильности и колебательных спектров изомеров β-каротина. Дж. Физ. хим. Б. 2010; 114:4366–4372. doi: 10.1021/jp911846h. [PubMed] [CrossRef] [Google Scholar]
45. Альфаро Р.А.Д., Гомес-Сандовал З., Маммино Л. Оценка антирадикальной активности гиперйовинола-А с использованием донорно-акцепторной карты. Дж. Мол. Модель. 2014;20:2337. дои: 10.1007/s00894-014-2337-й. [PubMed] [CrossRef] [Google Scholar]
46.
 Однако, как показывают результаты физических исследований, эти связи энергетически совершенно одинаковы. Следовательно, электронная пара, обусловливающая отрицательный заряд, не сосредоточена целиком на каком-либо одном кислородном атоме, а несколько смещена к азоту при одновременном смещении от азота ко второму кислородному атому подвижной π-электронной пары двойной связи. В результате выравнивания электронной плотности в нитрогруппе формальный отрицательный заряд (-1) распределяется поровну (-1/2) между обоими атоми кислорода:
Однако, как показывают результаты физических исследований, эти связи энергетически совершенно одинаковы. Следовательно, электронная пара, обусловливающая отрицательный заряд, не сосредоточена целиком на каком-либо одном кислородном атоме, а несколько смещена к азоту при одновременном смещении от азота ко второму кислородному атому подвижной π-электронной пары двойной связи. В результате выравнивания электронной плотности в нитрогруппе формальный отрицательный заряд (-1) распределяется поровну (-1/2) между обоими атоми кислорода:
Добавить комментарий